metodura comp, 100 mg/12,5 mg Tabletten
Jede Tablette enthält 100 mg Metoprololtartrat und 12,5 mg Hydrochlorothiazid.
Sonstiger Bestandteil mit bekannter Wirkung:
Jede Tablette enthält 80 mg Lactose-Monohydrat.
Vollständige Auflistung der sonstigen Bestandteile, siehe Abschnitt 6.1.
Tablette
metodura comp sind weiße, runde, beidseitig gewölbte Tabletten mit Markierungsrille auf einer Seite. Die Markierungsrille dient nicht zum Teilen der Tablette.
Arterielle Hypertonie
Das Kombinationspräparat metodura comp wird nur dann empfohlen, wenn die Therapie mit einem der Einzelwirkstoffe Metoprolol oder Hydrochlorothiazid, mit dem die Ersteinstellung eines zu hohen Blutdruckes versucht werden sollte, unzureichend wirkte und die Kombination der Einzelwirkstoffe in der in metodura comp vorliegenden Dosierung sich als gut dosiert erwiesen hat.
Grundsätzlich sollte die Behandlung eines zu hohen Blutdruckes mit niedrigen Dosen eines Einzelwirkstoffes einschleichend begonnen und langsam gesteigert werden. Die fixe Kombination metodura comp aus Metoprolol und Hydrochlorothiazid sollte erst angewendet werden, wenn durch die Einzelwirkstoffe keine Normalisierung des Blutdruckes bewirkt werden konnte oder bei hoher Dosierung übermäßige Nebenwirkungen aufgetreten waren und sich die Kombination der Einzelwirkstoffe in der in metodura comp vorliegenden Dosierung als gut dosiert erwiesen hat. Es gelten folgende Richtdosen:
Dosierung
Arterielle Hypertonie
In der Regel 1-mal 1 Tablette metodura comp (entsprechend 100 mg Metoprololtartrat und 12,5 mg Hydrochlorothiazid) täglich.
Bei gleichzeitig eingeschränkter Nieren- und Leberfunktion ist die Elimination des Metoprolol- Anteils von metodura comp vermindert, so dass unter Umständen eine Dosisreduktion erforderlich ist.
Die Dauer der Anwendung ist zeitlich nicht begrenzt. Sie richtet sich nach Art und Schwere der Erkrankung.
Nach Langzeitbehandlung sollte metodura comp - besonders bei Vorliegen einer ischämischen Herzkrankheit - ausschleichend (d. h. über 7-10 Tage) abgesetzt werden, da ein abruptes Absetzen zu einer akuten Verschlechterung des Zustandes des Patienten führen kann.
Art der Anwendung
Die Tabletten sind unzerkaut zum Frühstück mit ausreichend Flüssigkeit einzunehmen.
metodura comp darf nicht angewendet werden bei:
akutem Herzinfarkt
manifester Herzinsuffizienz
Schock
AV-Block 2. oder 3. Grades
Sinusknoten-Syndrom (sick sinus syndrome)
sinuatrialem Block
Bradykardie (Ruhepuls kleiner als 50 Schläge pro Minute vor Behandlungsbeginn)
Hypotonie, systolisch unter 90 mmHg
Azidose
bronchialer Hyperreagibilität (z. B. Asthma bronchiale)
Spätstadien peripherer Durchblutungsstörungen
gleichzeitiger Gabe von MAO-Hemmstoffen (Ausnahme MAO-B-Hemmstoffe)
schweren Nierenfunktionsstörungen (Niereninsuffizienz mit Oligurie oder Anurie; Kreatinin-Clearance kleiner als 30 ml/min und/oder Serum-Kreatinin über 1,8 mg/100 ml)
akuter Glomerulonephritis
Coma und Praecoma hepaticum
therapieresistenter Hypokaliämie (unter 3,5 mmol/l)
Hyponatriämie
Hypovolämie
Hyperkalzämie
Gicht
Überempfindlichkeit gegen die Wirkstoffe Hydrochlorothiazid und Metoprololtartrat, einen der in Abschnitt 6.1 genannten sonstigen Bestandteile des Arzneimittels, andere Thiaziddiuretika, andere Beta-Rezeptorenblocker sowie gegen Sulfonamide
Die intravenöse Applikation von Calciumantagonisten vom Verapamil- und Diltiazem- Typ oder anderen Antiarrhythmika (wie Disopyramid) bei Patienten die mit metodura comp behandelt werden, ist kontraindiziert (Ausnahme Intensivmedizin).
Eine besonders sorgfältige ärztliche Überwachung ist erforderlich bei:
AV-Block 1. Grades
manifestem oder latentem Diabetes mellitus (schwere hypoglykämische Zustände möglich; regelmäßige Kontrolle des Blutzuckers)
längerem strengen Fasten und schwerer körperlicher Belastung (wegen möglicher schwerer hypoglykämischer Zustände)
Patienten mit Phäochromozytom (Nebennierenmarktumor) (metodura comp erst nach vorheriger alpha-Blockade verabreichen)
zerebrovaskulären Durchblutungsstörungen
koronarer Herzkrankheit
eingeschränkter Nierenfunktion leichteren Grades (Serum-Kreatinin zwischen oberem Normalwert und 1,8 mg/100 ml bzw. leichter Einschränkung der Kreatinin-Clearance mit 30‑60 ml/min) und gleichzeitiger Einschränkung der Leberfunktion (Dosisanpassung).
Nicht-melanozytärer Hautkrebs
In zwei epidemiologischen Studien auf der Grundlage des dänischen nationalen Krebsregisters wurde ein erhöhtes Risiko von nicht-melanozytärem Hautkrebs (NMSC) [Basalzellkarzinom (BCC) und Plattenepithelkarzinom (SCC)] mit steigender kumulativer Dosis von Hydrochlorothiazid (HCTZ) beobachtet. Photosensibilisierende Wirkungen von HCTZ könnten zur Entstehung von NMSC beitragen.
Patienten, die HCTZ einnehmen, sollten über das NMSC-Risiko informiert werden, und es sollte ihnen geraten werden, ihre Haut regelmäßig auf neue Läsionen zu prüfen und unverzüglich alle verdächtigen Hautveränderungen zu melden. Den Patienten sollten mögliche vorbeugende Maßnahmen empfohlen werden, um das Risiko von Hautkrebs zu minimieren; z. B. Einschränkung der Exposition gegenüber Sonnenlicht und UV- Strahlung oder im Fall einer Exposition Verwendung eines angemessenen Sonnenschutzes. Verdächtige Hautveränderungen sollten unverzüglich untersucht werden, ggf. einschließlich histologischer Untersuchungen von Biopsien. Bei Patienten, bei denen bereits ein NMSC aufgetreten ist, sollte die Verwendung von HCTZ überprüft werden (siehe auch Abschnitt 4.8).
Bei Patienten mit einer Psoriasis in der Eigen- oder Familienanamnese sollte die Verordnung von Arzneimitteln, die Beta-Rezeptorenblocker enthalten, nur nach sorgfältiger Nutzen-Risiko-Abwägung erfolgen.
Akute Atemwegstoxizität
Es wurden sehr seltene schwere Fälle von akuter Atemwegstoxizität, einschließlich des akuten Atemnotsyndroms (ARDS), nach der Einnahme von Hydrochlorothiazid berichtet. Ein Lungenödem entwickelt sich typischerweise innerhalb von Minuten bis Stunden nach der Einnahme von Hydrochlorothiazid. Zu den Symptomen gehören zu Beginn Dyspnoe, Fieber, Verschlechterung der Lungenfunktion und Hypotonie. Bei Verdacht auf ARDS sollte metodura comp abgesetzt und eine angemessene Behandlung eingeleitet werden. Hydrochlorothiazid darf nicht bei Patienten angewendet werden, bei denen nach der Einnahme von Hydrochlorothiazid bereits einmal ein ARDS aufgetreten ist.
Beta-Rezeptorenblocker können die Empfindlichkeit gegenüber Allergenen und die Schwere anaphylaktischer Reaktionen erhöhen. Deshalb ist eine strenge Indikationsstellung bei Patienten mit schweren Überempfindlichkeitsreaktionen in der Vorgeschichte und bei Patienten unter Desensibilisierungstherapie (Vorsicht, überschießende anaphylaktische Reaktionen) geboten.
Die Therapie mit metodura comp sollte abgebrochen werden bei therapieresistenter Entgleisung des Elektrolythaushalts, orthostatischen Beschwerden (z.B. Schwarzwerden vor den Augen, Schwindel, evtl. Ohnmacht), Überempfindlichkeitsreaktionen, starken Beschwerden im Magen- oder Darmtrakt, zentralnervösen Störungen, Pankreatitis (Entzündungen der Bauchspeicheldrüse), Blutbildveränderungen, bei akuter Gallenblasenentzündung, beim Auftreten einer Gefäßentzündung (Vaskulitis) und Verschlimmerung einer bestehenden Kurzsichtigkeit.
Aderhauterguss (choroidaler Erguss), akute Myopie und sekundäres Winkelverschlussglaukom
Sulfonamide und Sulfonamid-Derivate können eine idiosynkratische Reaktion auslösen, die zu einem Aderhauterguss mit Gesichtsfelddefekt, transienter Myopie und zu einem akuten Winkelverschlussglaukom führen kann. Die Symptome beinhalten plötzliches Auftreten einer verminderten Sehschärfe oder Augenschmerzen und treten typischerweise innerhalb von Stunden bis Wochen nach Beginn der Einnahme auf. Ein unbehandeltes Engwinkelglaukoms kann zu einem permanenten Sehverlust führen. Die wichtigste Behandlung ist ein schnellstmöglicher Abbruch der Therapie. Umgehende medizinische oder chirurgische Behandlungen müssen möglicherweise in Betracht gezogen werden, wenn der Augeninnendruck weiterhin unkontrolliert ist. Risikofaktoren für die Entwicklung eines akuten Engwinkelglaukoms können eine in der Vergangenheit aufgetretene Allergie gegen Sulfonamide oder Penicillin einschließen.
Sonstige Hinweise
Während einer Langzeittherapie mit metodura comp sollten die Serumelektrolyte (insbesondere Kalium, Natrium, Calcium), Kreatinin und Harnstoff, die Serumlipide (Cholesterol und Triglyceride), die Harnsäure sowie der Blutzucker regelmäßig kontrolliert werden.
Während der Behandlung mit metodura comp sollten die Patienten auf eine ausreichende Flüssigkeitsaufnahme achten und wegen erhöhter Kaliumverluste kaliumreiche Nahrungsmittel zu sich nehmen (z. B. Bananen, Gemüse, Nüsse). Die Kaliumverluste können durch gleichzeitige Therapie mit kaliumsparenden Diuretika vermindert werden oder verhindert werden.
Die Anwendung von metodura comp kann bei Dopingkontrollen zu positiven Ergebnissen führen. Die Anwendung von metodura comp als Dopingmittel kann zu einer Gefährdung der Gesundheit führen.
Patienten mit der seltenen hereditären Galactose-Intoleranz, völligem Lactase-Mangel oder Glucose-Galactose-Malabsorption sollten metodura comp nicht einnehmen.
metodura comp enthält weniger als 1 mmol (23 mg) Natrium pro Tablette, d.h., es ist nahezu „natriumfrei“.
Folgende Wechselwirkungen zwischen dem vorliegenden und anderen Arzneimitteln sind zu beachten:
Durch den Wirkstoff Metoprololtartrat bedingte Wechselwirkungen:
Bei gleichzeitiger Anwendung von metodura comp und Calciumantagonisten vom Nifedipin-Typ kann es zu einer verstärkten Blutdrucksenkung und in Einzelfällen zur Ausbildung einer Herzinsuffizienz kommen.
Die kardiodepressiven Wirkungen von metodura comp und Antiarrhythmika können sich addieren.
Bei gleichzeitiger Anwendung von metodura comp und Calciumantagonisten vom Verapamil- oder Diltiazem-Typ oder anderen Antiarrhythmika (wie Disopyramid) ist eine sorgfältige Überwachung der Patienten angezeigt, da es zu Hypotension, Bradykardie oder anderen Herzrhythmusstörungen kommen kann.
Hinweis: Die intravenöse Applikation von Calciumantagonisten vom Verapamil- und Diltiazem-Typ oder anderen Antiarrhythmika (wie Disopyramid) bei Patienten, die mit metodura comp behandelt werden, ist kontraindiziert (Ausnahme Intensivmedizin).
Bei gleichzeitiger Anwendung von metodura comp und Herzglykosiden, Reserpin, alpha-Methyldopa, Guanfacin oder Clonidin kann es zu einem stärkeren Absinken der Herzfrequenz bzw. zu einer Verzögerung der Überleitung kommen.
Nach abruptem Absetzen von Clonidin bei gleichzeitiger Anwendung von metodura comp kann der Blutdruck überschießend ansteigen. Clonidin darf daher erst abgesetzt werden, wenn einige Tage zuvor die Verabreichung von metodura comp beendet wurde. Anschließend kann Clonidin stufenweise abgesetzt werden.
Bei gleichzeitiger Anwendung von metodura comp und Noradrenalin, Adrenalin oder anderen sympathomimetisch wirkenden Substanzen (z. B. enthalten in Hustenmitteln, Nasen- und Augentropfen) ist ein Blutdruckanstieg möglich.
Monoaminooxidase-(MAO)-Hemmer sollten wegen möglicher überschießender Hypertension nicht zusammen mit metodura comp eingenommen werden.
Die gleichzeitige Anwendung von metodura comp und Narkotika kann eine verstärkte Blutdrucksenkung zur Folge haben. Die negativ inotrope Wirkung der beiden vorgenannten Arzneimittel kann sich addieren.
Für den Fall, dass metodura comp vor Eingriffen in Allgemeinnarkose oder vor der Anwendung curareartiger Muskelrelaxantien nicht abgesetzt werden kann, muss der Narkosearzt über die Behandlung mit metodura comp informiert werden.
Rifampicin und Indometacin können die blutdrucksenkende Wirkung von metodura comp vermindern.
Die Wirkung von metodura comp kann durch Cimetidin verstärkt werden. metodura comp kann die Ausscheidung von Lidocain vermindern.
Durch den Wirkstoff Hydrochlorothiazid bedingte Wechselwirkungen:
Unter Behandlung mit metodura comp besteht bei zusätzlicher Einnahme von ACE-Hemmern (z. B. Captopril, Enalapril) zu Behandlungsbeginn das Risiko eines massiven Blutdruckabfalls und eine Verschlechterung der Nierenfunktion.
Salicylate und andere nichtsteroidale Antiphlogistika (z. B. Indometacin) können die antihypertensive und antidiuretische Wirkung von metodura comp vermindern. Bei hochdosierter Salicylateinnahme kann die toxische Wirkung der Salicylate auf das zentrale Nervensystem verstärkt werden. Bei Patienten, die unter metodura comp-Therapie eine Hypovolämie entwickeln, kann die gleichzeitige Gabe nichtsteroidaler Antiphlogistika ein akutes Nierenversagen auslösen.
Hinweis: Die Wirkung harnsäuresenkender Arzneimittel kann bei gleichzeitiger Anwendung von metodura comp abgeschwächt werden.
Bei gleichzeitiger Anwendung von metodura comp und Arzneimitteln, die zu Kalium- und Magnesiumverlusten führen, z. B. kaliuretische Diuretika, Kortikosteroide, Laxantien (chron. Abusus), Amphotericin B, Carbenoxolon, Penicillin G und Salicylate können Wirkungen und Nebenwirkungen von Herzglykosiden verstärkt werden.
Die gleichzeitige Gabe von metodura comp und Lithium führt über eine verminderte Lithiumausscheidung zu einer Verstärkung der kardio- und neurotoxischen Wirkung des Lithiums.
Bei gleichzeitiger Anwendung von Zytostatika (z. B. Cyclophosphamid, Fluorouracil, Methotrexat) ist mit verstärkter Knochenmarkstoxizität (insbesondere Granulozytopenie) zu rechnen.
Die gleichzeitige Anwendung von Cholestyramin oder Colestipol vermindert die Resorption des Hydrochlorothiazid-Anteils von metodura comp.
Bei gleichzeitiger Anwendung von Methyldopa sind in Einzelfällen Hämolysen durch Bildung von Antikörpern gegen Hydrochlorothiazid beschrieben worden.
metodura comp kann die Ausscheidung von Lidocain und Chinidin vermindern.
Hinweis:
Die Wirkung harnsäuresenkender Arzneimittel sowie von Adrenalin kann bei gleichzeitiger Anwendung von metodura comp abgeschwächt werden.
Die dämpfenden Wirkungen von metodura comp und Alkohol können sich gegenseitig verstärken.
Durch die Wirkstoffe Metoprololtartrat und Hydrochlorothiazid bedingte Wechselwirkungen:
Bei gleichzeitiger Anwendung von metodura comp und Insulin oder oralen Antidiabetika kann deren Wirkung sowohl verstärkt bzw. verlängert als auch abgeschwächt werden. Warnzeichen einer Hypoglykämie - insbesondere Tachykardie und Tremor - sind verschleiert oder abgemildert. Daher sind regelmäßige Blutzuckerkontrollen erforderlich.
Die blutdrucksenkende Wirkung von metodura comp kann durch andere blutdrucksenkende Arzneimittel, Barbiturate, Phenothiazine, trizyklische Antidepressiva, Vasodilatatoren oder durch Alkoholgenuss verstärkt werden.
Die Wirkung curareartiger Muskelrelaxantien kann durch metodura comp verstärkt und verlängert werden.
Warnhinweise
Arzneimittel, die Beta-Rezeptorenblocker enthalten, zeigen eine schwerere Verlaufsform des anaphylaktischen Schocks.
Schwangerschaft
Es liegen nur begrenzte Erfahrungen mit der Anwendung von Hydrochlorothiazid in der Schwangerschaft vor, insbesondere während des ersten Trimesters. Ergebnisse aus Tierstudien sind unzureichend (siehe Abschnitt 5.3). Die Anwendung von metodura comp während der Schwangerschaft und bei Frauen im gebärfähigen Alter, die nicht verhüten, wird nicht empfohlen.
Hydrochlorothiazid ist plazentagängig. Auf Grund des pharmakologischen Wirkmechanismus von Hydrochlorothiazid kann es bei Anwendung während des zweiten und dritten Trimesters zu einer Störung der feto-plazentaren Perfusion und zu fetalen und neonatalen Auswirkungen wie Ikterus, Störung des Elektrolythaushalts und Thrombozytopenien kommen.
Auf Grund des Risikos eines verringerten Plasmavolumens und einer plazentaren Hypoperfusion, ohne den Krankheitsverlauf günstig zu beeinflussen, sollte Hydrochlorothiazid bei Schwangerschaftsödemen, Schwangerschaftshypertonie oder einer Präeklampsie nicht zur Anwendung kommen.
Bei essentieller Hypertonie schwangerer Frauen sollte Hydrochlorothiazid nur in den seltenen Fällen, in denen keine andere Behandlung möglich ist, angewandt werden.
Stillzeit
Hydrochlorothiazid geht in geringen Mengen in die Muttermilch über. Thiazid-Diuretika, angewandt in hohen Dosen zur intensiven Diurese, können die Laktation hemmen. Die Anwendung von metodura comp während der Stillzeit wird nicht empfohlen. Wenn metodura comp während der Stillzeit angewandt wird, sollte die Dosis so niedrig wie möglich sein.
Die Behandlung des Bluthochdrucks mit diesem Arzneimittel bedarf der regelmäßigen ärztlichen Kontrolle. Durch individuell auftretende unterschiedliche Reaktionen kann die Fähigkeit zur aktiven Teilnahme am Straßenverkehr oder zum Bedienen von Maschinen beeinträchtigt werden. Dies gilt in verstärktem Maße bei Behandlungsbeginn, Dosiserhöhung und Präparatewechsel sowie im Zusammenwirken mit Alkohol.
Bei den Häufigkeitsangaben zu Nebenwirkungen werden folgende Kategorien zugrunde gelegt:
Sehr häufig (> 1/10)
Häufig (> 1/100 bis < 1/10)
Gelegentlich (> 1/1.000 bis < 1/100)
Selten (>1/10.000 bis < 1/1.000)
Sehr selten (<1/10.000)
Nicht bekannt (Häufigkeit auf Grundlage der verfügbaren Daten nicht abschätzbar).
Gutartige, bösartige und unspezifische Neubildungen (einschl. Zysten und Polypen)
Nicht bekannt: Nicht-melanozytärer Hautkrebs (Basalzellkarzinom und Plattenepithelkarzinom)
Erkrankungen des Nervensystems
Häufig kann es zu zentralnervösen Störungen wie Müdigkeit, depressiven Verstimmungen, Schwindelgefühl, Verwirrtheit, Kopfschmerzen, Schwitzen, Alpträumen oder verstärkter Traumaktivität, Schlafstörungen und Halluzinationen kommen; diese Erscheinungen sind gewöhnlich leichterer Art und vorübergehend.
Erkrankungen des Gastrointestinaltrakts
Häufig wurden Appetitlosigkeit und Magen-Darm-Beschwerden (z. B. Übelkeit, Erbrechen, Obstipation, Diarrhöe, Schmerzen und Krämpfe im Bauchraum) beobachtet.
Gelegentlich: Mundtrockenheit
Erkrankungen der Haut und des Unterhautzellgewebes
Allergische Hautreaktionen (z. B. Rötung, Juckreiz, photoallergisches Exanthem, Purpura, Urtikaria) können häufig auftreten.
Allergische Hauterscheinungen wie Pruritus, Hautrötung, Urtikaria, kutaner Lupus erythematodes und chronische Photosensibilität sowie Arzneimittelfieber und Ikterus sind gelegentlich bekannt geworden.
Herz-Kreislauf- und Gefäßerkrankungen
Häufig kann es zu Parästhesien und Kältegefühl an den Extremitäten, Muskelschwäche oder Muskelkrämpfen (z. B. Wadenkrämpfe) kommen.
Auch eine Verstärkung der Beschwerden bei Patienten mit peripheren Durchblutungsstörungen (einschließlich Patienten mit Raynaud-Syndrom) wurde beobachtet.
Die Behandlung mit metodura comp kann in gelegentlich zu verstärktem Blutdruckabfall, Synkopen, Palpitationen, Bradykardie, atrioventrikulären Überleitungsstörungen oder Verstärkung einer Herzinsuffizienz mit peripheren Ödemen und/oder Belastungsdyspnoe führen. Sehr selten ist bei Patienten mit Angina pectoris eine Verstärkung der Anfälle nicht auszuschließen.
Erkrankungen der Atemwege, des Brustraums und Mediastinums
Infolge einer möglichen Erhöhung des Atemwegswiderstandes kann es bei Patienten mit Neigung zu bronchospastischen Reaktionen (insbesondere bei obstruktiven Atemwegserkrankungen) zu Atemnot kommen.
Sehr selten wurde ein Akutes Atemnotsyndrom (ARDS) (siehe Abschnitt 4.4) beobachtet.
Augenerkrankungen
Gelegentlich wurden Konjunktivitis, verminderter Tränenfluss (dies ist beim Tragen von Kontaktlinsen zu beachten) sowie sehr selten Sehstörungen beobachtet.
Nicht bekannt: Aderhauterguss
Stoffwechsel und Ernährungsstörungen
Ein latenter Diabetes mellitus kann in Erscheinung treten bzw. ein bereits manifester Diabetes mellitus sich verschlechtern. Nach längerem strengen Fasten oder schwerer körperlicher Belastung kann es bei gleichzeitiger Therapie mit metodura comp zu hypoglykämischen Zuständen kommen. Warnzeichen einer Hypoglykämie (insbesondere Tachykardie und Tremor) können verschleiert werden.
Sehr selten wurde eine Erhöhung der Transaminasen (GOT, GPT) im Serum oder das Auftreten einer Hepatitis beobachtet.
Sehr häufig kommt es zu einer in der Regel asymptomatischen Hyperurikämie. Diese kann jedoch bei prädisponierten Patienten Gichtanfälle auslösen.
Sehr häufig kommt es unter Hydrochlorothiazid zu Erhöhung der Cholesterin- und Triglyzeridspiegel im Serum.
Sonstiges
Des Weiteren wurden sehr selten Haarausfall, Hörstörungen oder Ohrensausen, Gewichtszunahme, Persönlichkeitsveränderungen (z.B. Gefühlsschwankungen, kurzdauernder Gedächtnisverlust), eine Rhinitis allergica oder eine Induratio penis plastica (Peyronie's disease) beobachtet.
Gelegentlich kommt es zu einer Erhöhung der harnpflichtigen stickstoffhaltigen Substanzen (Azotämie).
Hyperamylasämien und Pankreatitiden sind gelegentlich aufgetreten, bei vorbestehender Cholelithiasis kann eine akute Cholezystitis auftreten. Sehr selten wurde unter Hydrochlorothiazid ein allergisches Lungenödem beobachtet (systemische anaphylaktische Reaktionen durch zirkulierende Immunkomplexe).
Erkrankungen der Geschlechtsorgane und der Brustdrüse
Sehr selten wurden Libido- und Potenzstörungen sowie das Auftreten einer Thrombozytopenie oder Leukopenie beobachtet.
Erkrankungen des Blutes und des Lymphsystems
Selten kann es zu Störungen im Fettstoffwechsel kommen. Bei meist normalem Gesamtcholesterin wurde eine Verminderung des HDL-Cholesterins und eine Erhöhung der Triglyzeride im Plasma beobachtet.
Sehr selten sind Veränderung im Blutbild folgender Art beschrieben worden: Aplastische Anämie, Leukopenie, Agranulozytose und sehr häufig Thrombozytopenien.
Sehr selten werden hämolytischen Anämien infolge einer Antikörperbildung gegen Hydrochlorothiazid beschrieben.
Skelettmuskulatur-, Bindegewebs- und Knochenerkrankungen
Unter einer Therapie mit Metoprololtartrat (Wirkstoff in metodura comp) wurde sehr selten eine Arthropathie (Mono- und Polyarthritis) beobachtet
Flüssigkeits- und Elektrolythaushalt
Aufgrund des Hydrochlorothiazid-Anteils treten bei der Anwendung von metodura comp sehr häufig dosis- und altersabhängig Wasser und Elektrolytstörungen auf, insbesondere Hypokaliämie und Hypochlorämie sowie Hyperkalzämie. Als Folge von Elektrolyt- und Flüssigkeitsverlusten kann sich eine metabolische Alkalose entwickeln bzw. eine bereits bestehende metabolische Alkalose kann sich verschlechtern. Dabei treten Allgemeinsymptome wie Mundtrockenheit, Durst, Müdigkeit, Benommenheit, Schläfrigkeit, Schwäche, Schwindel, Hypotonie und orthostatische Regulationsstörungen auf.
Bei exzessiver Diurese kann es infolge Dehydratation und Hypovolämie zur Hämokonzentration und gelegentlich zu Konvulsionen, Benommenheit, Verwirrtheitszuständen, Kreislaufkollaps und zu einem akuten Nierenversagen sowie als Folge der Hämokonzentration - insbesondere bei älteren Patienten oder bei Vorliegen von Venenerkrankungen - zu Thrombosen und Embolien kommen.
Sehr häufig können Hypokaliämien auftreten, die Symptome wie Übelkeit, Erbrechen, Apathie, Hypotonie der Skelettmuskulatur, Adynamie der glatten Muskulatur mit Obstipation sowie Subileus bis hin zum paralytischen Ileus sowie EKG-Veränderungen verursachen.
Herzrhythmusstörungen und eine gesteigerte Glykosidempfindlichkeit können unter Hydrochlorothiazid sehr häufig eintreten.
Hypermagnesiurien sind sehr häufig und äußern sich gelegentlich als Hypomagnesiämien, weil Magnesium aus dem Knochen mobilisiert wird.
Sehr häufig treten unter Hydrochlorothiazid Hyperglykämie und Glukosurie bei Stoffwechselgesunden, bei Patienten mit latentem oder manifestem Diabetes mellitus bzw. Patienten mit Kaliummangel auf.
Außerdem sind anaphylaktoide Reaktionen, Aggravierung eines akuten Nierenversagens sowie abakterielle interstitielle Nephritiden mit konsekutivem akuten Nierenversagen sehr selten bekannt geworden.
Beschreibung ausgewählter Nebenwirkungen
Nicht-melanozytärer Hautkrebs: Auf der Grundlage der vorliegenden Daten aus epidemiologischen Studien wurde ein kumulativer dosisabhängiger Zusammenhang zwischen HCTZ und NMSC festgestellt (siehe auch Abschnitt 4.4 und 5.1).
Meldung des Verdachts auf Nebenwirkungen
Die Meldung des Verdachts auf Nebenwirkungen nach der Zulassung ist von großer Wichtigkeit. Sie ermöglicht eine kontinuierliche Überwachung des Nutzen-Risiko-Verhältnisses des Arzneimittels. Angehörige von Gesundheitsberufen sind aufgefordert, jeden Verdachtsfall einer Nebenwirkung dem Bundesinstitut für Arzneimittel und Medizinprodukte, Abt. Pharmakovigilanz, Kurt-Georg-Kiesinger-Allee 3, D-53175 Bonn, Website: www.bfarm.de anzuzeigen.
a) Symptome der Intoxikation
Metoprolol
Das klinische Bild ist in Abhängigkeit vom Ausmaß der Intoxikation im Wesentlichen von kardiovaskulären und zentralnervösen Symptomen geprägt. Überdosierung kann zu schwerer Hypotonie, Bradykardie bis zum Herzstillstand, Herzinsuffizienz und kardiogenem Schock führen. Zusätzlich können Atembeschwerden, Bronchospasmen, Erbrechen, Bewusstseinsstörungen, gelegentlich auch generalisierte Krampfanfälle auftreten.
Hydrochlorothiazid
Das klinische Bild bei akuter oder chronischer Überdosierung ist vom Ausmaß des Flüssigkeits- und Elektrolytverlustes abhängig.
Überdosierung kann bei ausgeprägten Flüssigkeits- und Natriumverlusten zu Durst, Schwäche- und Schwindelgefühl, Muskelschmerzen und Muskelkrämpfen (z. B. Wadenkrämpfe), Kopfschmerzen, Tachykardie, Hypotonie und orthostatischen Regulationsstörungen, infolge Dehydratation und Hypovolämie zur Hämokonzentration, zu Konvulsionen, Benommenheit, Lethargie, Verwirrtheitszuständen, Kreislaufkollaps und zu einem akuten Nierenversagen führen.
Infolge einer Hypokaliämie kann es zu Müdigkeit, Muskelschwäche, Parästhesien, Paresen, Apathie, Meteorismus und Obstipation oder zu Herzrhythmusstörungen kommen. Schwere Kaliumverluste können zu einem paralytischen Ileus oder zu Bewusstseinsstörungen bis zum hypokaliämischen Koma führen.
b) Therapie von Intoxikationen
Bei Anzeichen einer Überdosierung oder bedrohlichem Abfall der Herzfrequenz und/ oder des Blutdrucks muss die Behandlung mit metodura comp umgehend abgesetzt werden.
Bei nur kurze Zeit zurückliegender Einnahme kann durch Maßnahmen der primären Giftelimination (induziertes Erbrechen, Magenspülung) oder resorptionsmindernde Maßnahmen (medizinische Kohle) versucht werden, die systemische Aufnahme von metodura comp zu vermindern.
Unter intensivmedizinischen Bedingungen müssen neben der Überwachung der vitalen Parameter wiederholt Kontrollen des Wasser- und Elektrolythaushalts, des Säure- Basen-Haushalts, des Blutzuckers und der harnpflichtigen Substanzen durchgeführt werden und Abweichungen gegebenenfalls korrigiert werden.
Als Gegenmittel können gegeben werden:
Atropin: 0,5-2,0 mg intravenös als Bolus.
Glukagon: initial 1-10 mg intravenös, anschließend 2-2,5 mg pro Std. als Dauerinfusion
Sympathomimetika in Abhängigkeit von Körpergewicht und Effekt: Dopamin, Dobutamin, Isoprenalin, Orciprenalin und Adrenalin.
Bei therapierefraktärer Bradykardie sollte eine temporäre Schrittmachertherapie durchgeführt werden.
Bei Bronchospasmen können β2-Sympathomimetika als Aerosol (bei ungenügender Wirkung auch intravenös) oder Aminophyllin i.v. gegeben werden.
Bei generalisierten Krampfanfällen empfiehlt sich die langsame intravenöse Gabe von Diazepam.
bei Hypovolämie: Volumensubstitution
bei Hypokaliämie: Kaliumsubstitution
bei Kreislaufkollaps: Schocklagerung, ggf. Schocktherapie
Pharmakotherapeutische Gruppe: Antihypertensivum, Kombination aus Beta-Rezeptorenblocker und Diuretikum
ATC-Code: C07BB02
Metoprolol:
Metoprolol ist ein schwach lipophiler Beta-Rezeptorenblocker mit relativer β1-Selektivität (Kardioselektivität), ohne intrinsische sympathomimetische Aktivität (ISA) und nur schwach ausgeprägter membranstabilisierender Wirkung.
Die Substanz senkt in Abhängigkeit von der Höhe des Sympathikustonus die Frequenz und die Kontraktionskraft des Herzens, die AV-Überleitungsgeschwindigkeit und die Plasma-Renin-Aktivität. Metoprolol kann durch Hemmung von β2-Rezeptoren eine Erhöhung des Tonus der glatten Muskulatur bewirken.
Hydrochlorothiazid:
Hydrochlorothiazid ist ein Benzothiadiazid. Thiazide wirken direkt an den Nieren, indem sie die Natriumchlorid- und die damit verbundene Wasserausscheidung vermehren. Ihr klinisch relevanter Hauptangriffsort ist der frühdistale Tubulus. Dort hemmen sie den elektroneutralen NaCl-Cotransport in der luminalen Zellmembran. Kalium und Magnesium werden vermehrt, Kalzium vermindert ausgeschieden. Hydrochlorothiazid bewirkt eine geringe Bicarbonatausscheidung und die Chloridausscheidung überschreitet die Ausscheidung des Natriums. Unter Hydrochlorothiazid kann sich eine metabolische Alkalose entwickeln. Hydrochlorothiazid wird wie andere organische Säuren aktiv im proximalen Tubulus sezerniert. Die diuretische Wirkung bleibt bei metabolischer Azidose oder metabolischer Alkalose erhalten.
Als Mechanismen der antihypertensiven Wirkung werden ein veränderter Natriumhaushalt, eine Reduktion des extrazellulären Wasser- und Plasmavolumens, eine Änderung des renalen Gefäßwiderstandes sowie eine reduzierte Ansprechbarkeit auf Norepinephrin und Angiotensin II diskutiert.
Metoprolol
Nach oraler Applikation wird Metoprolol nahezu vollständig (ca. 95 %) aus dem Gastrointestinaltrakt resorbiert. Da Metoprolol einem ausgeprägten First-pass-Metabolismus unterliegt, beträgt die systemische Verfügbarkeit nur ca. 50 %. Maximale Plasmaspiegel werden nach 1,5 – 2 Stunden erreicht.
Die Plasmaproteinbindung liegt bei ca. 12 %; das relative Verteilungsvolumen beträgt 5,6 l/kg.
Metoprolol wird fast vollständig in der Leber metabolisiert. Zwei der drei Hauptmetaboliten zeigten schwach betarezeptorenblockierende Eigenschaften, sind jedoch klinisch nicht relevant. Bei Leberzirrhose muss wegen der dann verminderten Metabolisierungsrate mit erhöhten Plasmaspiegeln an unverändertem Metoprolol gerechnet werden.
Metoprolol und seine Metabolite werden zu ca. 95 % — davon ca. 10 % unverändert — renal eliminiert. Die Eliminationshalbwertszeit von Metoprolol beträgt 3 – 5 Stunden.
Hydrochlorothiazid
Hydrochlorothiazid wird nach oraler Gabe zu 60-75 % resorbiert. Nach 25 mg p.o. Hydrochlorothiazid werden Plasmaspitzenkonzentrationen von 142 ng/ml nach 2-5 Stunden erreicht, nach 50 mg p.o. Hydrochlorothiazid 260 ng/ml nach 2-4 Stunden.
Hydrochlorothiazid wird zu 65 % an Plasmaproteine gebunden.
Die Elektrolyt- und Wasserausscheidung setzt nach 2 Stunden ein, erreicht ein Wirkungsmaximum nach 3-6 Stunden und hält 6-12 Stunden an. Bei antihypertensiver Anwendung tritt eine Wirkung erst nach 3-4 Tagen ein und kann bis zu einer Woche nach Therapieende anhalten.
Hydrochlorothiazid wird nahezu vollständig unverändert renal ausgeschieden (> 95 %), nach oraler Einzeldosis werden 50-70 % der Dosis in 24 Stunden ausgeschieden, bereits nach 60 Minuten erschienen nachweisbare Mengen im Urin.
Die Eliminationshalbwertszeit beträgt 6-8 Stunden.
Bei Niereninsuffizienz tritt eine Abnahme der Ausscheidung und eine Verlängerung der HWZ ein. Die renale Clearance von Hydrochlorothiazid zeigt dabei eine enge Korrelation zur Kreatinin-Clearance. Bei Patienten mit Restfiltraten (< 10 ml/min GFR) konnten nur noch 10 % der verabfolgten Dosis im Urin nachgewiesen werden. Neuere Untersuchungen weisen auf kompensatorische extrarenale Eliminationswege hin (Galle).
Bei Leberzirrhose zeigte sich keine relevante Veränderung der Pharmakokinetik von Hydrochlorothiazid. Untersuchungen der Kinetik von Hydrochlorothiazid bei Patienten mit Herzinsuffizienz liegen nicht vor.
Toxikologische Eigenschaften
Akute Toxizität
Metoprolol
Ratte (i.v.) LD50: 70 mg/kg/KG
Ratte (oral) LD50: 4000 mg/kg/KG
Hydrochlorothiazid
Die Prüfung der akuten Toxizität im Tierversuch hat keine besondere Empfindlichkeit ergeben.
Chronische Toxizität/Subchronische Toxizität
Untersuchungen zur chronischen Toxizität (6 Monate) an Ratte und Hund mit der Kombination Metoprolol und Hydrochlorothiazid ergaben keine Hinweise auf substanzspezifische additive oder überadditive toxische Effekte.
Mutagenes und tumorerzeugendes Potential
Die Kombination von Metoprolol und Hydrochlorothiazid wurde nicht bezüglich mutagene und tumorerzeugende Wirkungen geprüft.
Metoprolol
Metoprolol wurde keiner ausführlichen Mutagenitätsprüfung unterzogen; bisherige Untersuchungen ergaben keine Hinweise auf ein mutagenes Potential. Es liegen Ergebnisse von Kanzerogenitätsstudien an Ratten und Mäusen vor, aus denen sich kein tumorerzeugendes Potential ableiten lässt.
Hydrochlorothiazid
In-vitro- und in-vivo-Mutagenitätstests zur Induktion von Gen- und Chromosomenmutationen durch Hydrochlorothiazid verliefen negativ.
Langzeituntersuchungen an Ratten und Mäusen ergaben keinen Hinweis auf ein tumorerzeugendes Potential von Hydrochlorothiazid.
Nicht-melanozytärer Hautkrebs: Auf der Grundlage der vorliegenden Daten aus epidemiologischen Studien wurde ein kumulativer dosisabhängiger Zusammenhang zwischen HCTZ und NMSC beobachtet. Eine Studie umfasste eine Grundgesamtheit aus 71 533 Fällen von BCC und 8 629 Fällen von SCC mit Kontrollgruppen von 1 430 833 bzw. 172 462 Personen. Eine hohe HCTZ-Dosierung (≥ 50 000 mg kumulativ) war assoziiert mit einer bereinigten Odds-Ratio von 1,29 (95% Konfidenzintervall: 1,23-1,35) für BCC und 3,98 (95 % Konfidenzintervall: 3,68-4;31) für SCC. Sowohl bei BCC als auch bei SCC wurde eine eindeutige kumulative Dosis-Wirkungsbeziehung ermittelt. Eine weitere Studie ergab einen möglichen Zusammenhang zwischen Lippenkrebs (SCC) und der Exposition gegenüber HCTZ: 633 Fälle von Lippenkrebs wurden mittels eines risikoorientierten Stichprobenverfahrens mit einer Kontrollgruppe von 63 067 Personen abgeglichen. Es wurde eine kumulative Dosis-Wirkungsbeziehung mit einer bereinigten Odds-Ratio von 2,1 (95% Konfidenzintervall: 1,7-2,6) festgestellt, die sich bei hoher Exposition (~ 25 000 mg) auf eine Odds-Ratio von 3,9 (3,0-4,9) und bei der höchsten kumulativen Dosis (~ 100,000 mg) auf eine Odds-Ratio von 7,7 (5,7-10,5) erhöhte (siehe auch Abschnitt 4.4).
Zur Anwendung der Kombination in der Schwangerschaft und Stillzeit liegen für den Menschen keine Erfahrungen vor.
Metoprolol
Untersuchungen an zwei Tierspezies (Ratte, Kaninchen) haben keine Hinweise auf teratogene Eigenschaften von Metoprolol ergeben.
Für den Menschen liegen keine Erkenntnisse über die Sicherheit einer Anwendung im 1. und 2. Trimenon der Schwangerschaft vor.
Bei einer Anwendung von Metoprolol in den letzten drei Monaten der Schwangerschaft sind bei bisher ca. 100 Mutter-Kind-Paaren keine Schädigungen der Neugeborenen beobachtet worden.
Metoprolol durchdringt die Plazenta. Zum Zeitpunkt der Geburt sind die Serumkonzentrationen von Mutter und Kind vergleichbar. In der Muttermilch erreicht Metoprolol das Dreifache der gleichzeitig bei der Mutter gemessenen Serumkonzentration. Bei täglicher Einnahme von 200 mg Metoprolol werden ca. 225 mg pro Liter Milch ausgeschieden.
Hydrochlorothiazid
Hydrochlorothiazid passiert im Tierversuch die Plazenta. Untersuchungen an drei Tierarten (Ratte, Maus, Kaninchen) ergaben keine Hinweise auf eine teratogene Wirkung.
Beim Menschen liegen Erfahrungen für über 7500 Mutter-Kind-Paare vor. Davon wurden 107 im ersten Trimenon exponiert. Es besteht der Verdacht, dass bei Verwendung in der 2. Hälfte der Schwangerschaft bei Neugeborenen eine Thrombozytopenie ausgelöst werden kann.
Auswirkungen von Störungen des Elektrolythaushalts der Schwangeren auf den Feten sowie eine verminderte Plazentadurchblutung sind möglich.
Hydrochlorothiazid geht in geringen Mengen in die Muttermilch über. Thiazid-Diuretika können die Laktation hemmen.
Povidon K25
Lactose-Monohydrat
Maisstärke
Carboxymethylstärke-Natrium (Typ A) (Ph.Eur.)
Mikrokristalline Cellulose
Hochdisperses Siliciumdioxid
Magnesiumstearat (Ph.Eur.)
Nicht zutreffend.
2 Jahre
Nicht über 25 °C lagern.
Blisterpackungen (PVC/PVDC) mit 30, 50 und 100 Tabletten. Es werden möglicherweise nicht alle Packungsgrößen in den Verkehr gebracht.
Keine besonderen Anforderungen.
Mylan Germany GmbH
Lütticher Straße 5
53842 Troisdorf
Mitvertrieb:
Viatris Healthcare GmbH
Lütticher Straße 5
53842 Troisdorf
29859.00.00
Datum der Erteilung der Zulassung: 4. März 1993
Datum der letzten Verlängerung der Zulassung: 19. Juli 2005
Juni 2024
Verschreibungspflichtig
Zusätzliche Angaben der Firma Mylan Germany GmbH
zur Bioverfügbarkeit von metodura comp, Tabletten
13.4 Bioverfügbarkeit
Eine im Jahr 1989 durchgeführte Bioverfügbarkeitsuntersuchung an 20 Probanden ergab im Vergleich zum Referenzpräparat:
Metoprololtartrat:
metodura comp | Referenzpräparat | |
maximale Plasmakonzentration |
|
|
Zeitpunkt der maximalen Plasmakonzentration |
|
|
Fläche unter der Konzentrations- Zeit-Kurve |
|
|
Angabe der Werte als Mittelwerte und Standardabweichung.
Mittlere Plasmaspiegelverläufe im Vergleich zu einem Referenzpräparat in einem Konzentrations- Zeit-Diagramm (Abb.1):
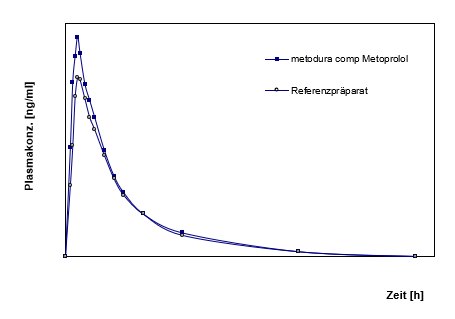
Hydrochlorothiazid:
metodura comp | Referenzpräparat | |
maximale Plasmakonzentration |
|
|
Zeitpunkt der maximalen Plasmakonzentration |
|
|
Fläche unter der Konzentrations- Zeit-Kurve |
|
|
Angabe der Werte als Mittelwerte und Standardabweichung.
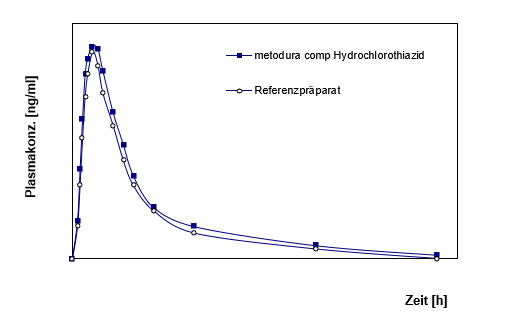
Mittlere Plasmaspiegelverläufe im Vergleich zu einem Referenzpräparat in einem Konzentrations- Zeit-Diagramm (Abb. 2):