▼Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung. Dies ermöglicht eine schnelle Identifizierung neuer Erkenntnisse über die Sicherheit. Angehörige von Gesundheitsberufen sind aufgefordert, jeden Verdachtsfall einer Nebenwirkung zu melden. Hinweise zur Meldung von Nebenwirkungen, siehe Abschnitt 4.8.
WELIREG® 40 mg Filmtabletten
Jede Filmtablette enthält 40 mg Belzutifan.
Vollständige Auflistung der sonstigen Bestandteile, siehe Abschnitt 6.1.
Filmtablette (Tablette).
Blaue, ovale Tablette, ungefähr 13 x 8 mm, auf einer Seite mit der Prägung „177“ versehen.
Nierenzellkarzinom (Renal Cell Carcinoma, RCC)
WELIREG ist als Monotherapie zur Behandlung des fortgeschrittenen klarzelligen Nierenzellkarzinoms bei Erwachsenen angezeigt, deren Erkrankung nach zwei oder mehreren Therapien, darunter ein PD-(L)1-Inhibitor und mindestens zwei zielgerichtete VEGF-Therapien, fortgeschritten ist.
Von Hippel-Lindau-Syndrom(VHL)-assoziierte Tumoren
WELIREG ist als Monotherapie zur Behandlung des von Hippel-Lindau-Syndroms bei Erwachsenen angezeigt, die eine Therapie für assoziierte lokale Nierenzellkarzinome (RCC), Hämangioblastome des Zentralnervensystems (ZNS) oder neuroendokrine Pankreastumoren (pNET) benötigen und für die lokale Therapien ungeeignet sind.
Die Therapie muss von in der Krebsbehandlung erfahrenen Fachärzten eingeleitet und überwacht werden.
Dosierung
Die empfohlene Dosis von WELIREG beträgt 120 mg Belzutifan (drei 40-mg-Tabletten), die einmal täglich, jeden Tag zur gleichen Zeit, eingenommen werden.
Die Behandlung sollte so lange fortgesetzt werden, bis die Krankheit fortschreitet oder eine unzumutbare Toxizität auftritt.
Versäumte Dosis
Wurde die Einnahme einer Dosis WELIREG versäumt, kann diese am gleichen Tag so bald wie möglich nachgeholt werden. Am nächsten Tag sollte die reguläre Tagesdosis wieder aufgenommen werden. Es sollten keine zusätzlichen Tabletten eingenommen werden, um die vergessene Dosis nachzuholen.
Falls nach der Einnahme von WELIREG erbrochen wird, sollte keine erneute Einnahme erfolgen, sondern die nächste Dosis am nächsten Tag eingenommen werden.
Dosisanpassung
Die Anpassung der Dosis von WELIREG bei Nebenwirkungen ist in Tabelle 1 zusammengefasst.
Tabelle 1: Empfehlungen zur Dosisanpassung
Nebenwirkungen |
Schweregrad* |
Dosisanpassung |
Anämie |
Grad 3 (Hämoglobin |
|
Grad 4 (lebensbedrohliche Folgen oder dringendes Eingreifen erforderlich) |
|
|
Hypoxie |
Grad 3 |
|
Grad 3 |
|
|
Grad 4 |
|
|
Andere Nebenwirkungen |
Grad 3 |
|
Grad 4 |
|
|
* Basierend auf National Cancer Institute Common Terminology Criteria for Adverse Events (NCI CTCAE), version 5.0 | ||
Besondere Patientengruppen
Ältere Patienten
Eine Dosisanpassung bei älteren Patienten ist nicht erforderlich (siehe Abschnitt 5.2).
Nierenfunktionsstörung
Eine Dosisanpassung bei Patienten mit Nierenfunktionsstörung, einschließlich terminaler Nierenerkrankung, ist nicht erforderlich (siehe Abschnitt 5.2).
Leberfunktionsstörung
Eine Dosisanpassung bei Patienten mit leichter (Gesamtbilirubin ≤ oberer Normwert [Upper Limit of Normal, ULN] und Aspartataminotransferase [AST] > ULN oder Gesamtbilirubin > 1 bis 1,5 x ULN und beliebiger AST) oder mittelschwerer (Gesamtbilirubin im Bereich von > 1,5 x ULN und ≤ 3 x ULN und beliebiger AST oder Child-Pugh B) Leberfunktionsstörung ist nicht erforderlich. Belzutifan wurde bei Patienten mit schwerer Leberfunktionsstörung nicht untersucht (siehe Abschnitt 5.2).
Kinder und Jugendliche
Die Sicherheit und Wirksamkeit bei Kindern im Alter von unter 18 Jahren ist nicht erwiesen (siehe Abschnitt 5.1). Es liegen keine Daten vor.
Art der Anwendung
WELIREG ist zum Einnehmen bestimmt.
Die Tabletten sind im Ganzen zu schlucken und können unabhängig von den Mahlzeiten eingenommen werden. Die Tabletten sollen nicht geteilt, zerkleinert oder gekaut werden, da nicht bekannt ist, ob dies die Resorption von Belzutifan beeinflusst.
Überempfindlichkeit gegen den Wirkstoff oder einen der in Abschnitt 6.1 genannten sonstigen Bestandteile.
Schwangerschaft bei Patientinnen mit VHL-Syndrom-assoziierten Tumoren (siehe Abschnitt 4.6).
Anämie
Bei Patienten, die in klinischen Studien Belzutifan erhielten, wurde über Anämie berichtet (siehe Abschnitt 4.8).
Die Patienten sollten vor Beginn der Behandlung mit Belzutifan und in regelmäßigen Abständen während der Behandlung auf Anämie überwacht werden. Bei Patienten, bei denen eine Anämie Grad 3 auftritt, sollte die Behandlung mit Belzutifan unterbrochen werden und die Patienten sollten gemäß der üblichen medizinischen Praxis behandelt werden, einschließlich der Gabe von Erythropoese-stimulierenden Mitteln (Erythropoiesis-Stimulating-Agents, ESAs), bis eine Besserung auf ≤ Grad 2 erfolgt ist (weitere Informationen finden Sie in den Fachinformationen für ESAs). Bei wiederkehrender Anämie Grad 3 sollte die Behandlung mit Belzutifan abgesetzt werden. Bei Patienten, bei denen eine Anämie Grad 4 auftritt, sollte die Behandlung mit Belzutifan unterbrochen und bei wiederkehrender Anämie Grad 4 dauerhaft abgesetzt werden (siehe Abschnitt 4.2).
Hypoxie
Bei Patienten, die in klinischen Studien Belzutifan erhielten, wurde über Hypoxie berichtet (siehe Abschnitt 4.8). Die Sauerstoffsättigung der Patienten sollte vor Beginn der Behandlung mit Belzutifan und in regelmäßigen Abständen während der Behandlung mittels Pulsoximetrie überwacht werden. Bei asymptomatischer Hypoxie Grad 3 sollten Sauerstoffzufuhr und die Fortsetzung oder Unterbrechung der Behandlung in Betracht gezogen werden. Wurde die Behandlung unterbrochen, sollte die Behandlung mit Belzutifan mit reduzierter Dosis fortgesetzt werden. Bei Patienten mit symptomatischer Hypoxie Grad 3 sollte die Behandlung mit Belzutifan unterbrochen, die Hypoxie behandelt und die Behandlung mit Belzutifan mit reduzierter Dosis fortgesetzt werden. Wenn die symptomatische Hypoxie weiterhin auftritt, sollte die Behandlung abgesetzt werden. Bei Hypoxie Grad 4 sollte die Behandlung dauerhaft abgesetzt werden (siehe Abschnitt 4.2).
Embryofetale Toxizität: Frauen im gebärfähigen Alter
Belzutifan kann beim Menschen embryofetale Schäden sowie eine Fehlgeburt verursachen (siehe Abschnitte 4.6 und 5.3).
Bei Frauen im gebärfähigen Alter muss vor Beginn der Behandlung mit Belzutifan ein Schwangerschaftstest durchgeführt werden.
Aufgrund des potenziellen Risikos für den Fötus müssen Frauen im gebärfähigen Alter während der Behandlung mit Belzutifan und mindestens 1 Woche nach der letzten Dosis hochwirksame Verhütungsmethoden anwenden (siehe Abschnitte 4.5 und 4.6).
ZNS-Blutungen bei Patienten mit VHL-Syndrom-assoziierten Hämangioblastomen des ZNS
ZNS-Blutungen, auch mit tödlichem Ausgang, wurden bei Patienten mit VHL-Syndrom-assoziierten Hämangioblastomen des ZNS beobachtet. Ärzte sollten bei Patienten mit VHL-Syndrom-assoziierten Hämangioblastomen des ZNS, die mit Belzutifan behandelt werden, auf Symptome oder Anzeichen von ZNS-Blutungen achten.
Informationen zu sonstigen Bestandteilen des Arzneimittels − Natrium
Dieses Arzneimittel enthält weniger als 1 mmol Natrium (23 mg) pro Tablette, d. h., es ist nahezu „natriumfrei“.
In-vitro- und pharmakogenomische Studien zeigen, dass Belzutifan durch UGT2B17 und CYP2C19 metabolisiert wird und dass Belzutifan CYP3A4 konzentrationsabhängig induziert.
Wirkung von Belzutifan auf andere Arzneimittel
Die gleichzeitige Gabe von Belzutifan mit CYP3A4-Substraten, einschließlich hormoneller Kontrazeptiva, verringert die Konzentrationen von CYP3A4-Substraten, was die Wirksamkeit dieser Substrate verringern kann. Das Ausmaß dieser Verringerung kann bei Patienten, die langsame duale UGT2B17- und CYP2C19-Metabolisierer sind, stärker ausgeprägt sein (siehe Abschnitt 5.2). Die gleichzeitige Gabe von Belzutifan mit empfindlichen CYP3A4-Substraten, bei denen eine minimale Konzentrationsabnahme zum Therapieversagen des Substrats führen kann, sollte vermieden werden. Wenn sich die gleichzeitige Gabe nicht vermeiden lässt, erhöhen Sie die Dosis des empfindlichen CYP3A4-Substrats gemäß der Zusammenfassung der Merkmale des Arzneimittels.
Die gleichzeitige Gabe von Belzutifan mit hormonellen Kontrazeptiva kann zu einem Versagen der Empfängnisverhütung (siehe Abschnitte 4.4 und 4.6) oder vermehrten Durchbruchblutungen führen. Patientinnen, die hormonelle Kontrazeptiva verwenden, sind anzuweisen, während der Behandlung mit Belzutifan eine alternative nicht-hormonelle Verhütungsmethode anzuwenden, oder ihr männlicher Partner muss ein Kondom anwenden.
In einer klinischen Studie führte die wiederholte Gabe von täglich 120 mg Belzutifan zu einer 40%igen Verringerung der Midazolam Fläche unter der Kurve (area under the curve, AUC), ein Effekt, der mit einem schwachen CYP3A4-Induktor übereinstimmt. Die Gabe von Belzutifan kann bei Patienten mit höherer Belzutifan-Plasmaexposition zu einer moderaten CYP3A4-Induktion führen (siehe Abschnitt 5.2).
Basierend auf In-vitro-Daten ist bei klinisch relevanten Expositionen durch Belzutifan eine Hemmung von MATE2-K zu erwarten und eine Hemmung von MATE1 kann nicht ausgeschlossen werden.
Belzutifan ist in vitro ein CYP2B6- und CYP2C8-Induktor. In-vivo-Untersuchungen wurden nicht durchgeführt. Die gleichzeitige Verabreichung mit Belzutifan kann zu einer klinisch relevanten Abnahme der Plasmakonzentration empfindlicher CYP2B6- und/oder CYP2C8-Substrate führen.
Auswirkungen anderer Arzneimittel auf Belzutifan
Die gleichzeitige Gabe von Belzutifan mit UGT2B17- oder CYP2C19-Inhibitoren erhöht die Plasmakonzentration von Belzutifan, was die Häufigkeit und Schwere der Nebenwirkungen von Belzutifan erhöhen kann. Patienten sind auf Anämie und Hypoxie zu überwachen und die Dosis von Belzutifan ist, wie empfohlen, zu reduzieren.
Die Auswirkungen starker CYP2C19-Induktoren auf die Belzutifan-Exposition wurden noch nicht untersucht.
Frauen im gebärfähigen Alter/Empfängnisverhütung bei Männern und Frauen
Bei Frauen im gebärfähigen Alter muss vor Beginn der Behandlung mit Belzutifan ein Schwangerschaftstest durchgeführt werden.
Belzutifan kann bei Gabe an eine schwangere Frau embryofetale Schäden sowie eine Fehlgeburt verursachen (siehe Abschnitte 4.4 und 5.3). Frauen im gebärfähigen Alter sind über das potenzielle Risiko für den Fötus zu informieren.
Frauen im gebärfähigen Alter müssen während der Behandlung mit Belzutifan und für mindestens 1 Woche nach der letzten Dosis hochwirksame Verhütungsmethoden anwenden. Die Anwendung von Belzutifan kann die Wirksamkeit hormoneller Kontrazeptiva verringern. Patientinnen, die hormonelle Kontrazeptiva verwenden, sind anzuweisen, während der Behandlung mit Belzutifan eine alternative nicht-hormonelle Verhütungsmethode anzuwenden, oder ihr männlicher Partner muss ein Kondom anwenden (siehe Abschnitt 4.5).
Schwangerschaft
Es liegen keine oder nur begrenzte Daten zur Anwendung von Belzutifan bei schwangeren Frauen vor. Tierexperimentelle Studien haben eine Reproduktionstoxizität gezeigt (siehe Abschnitt 5.3).
Nierenzellkarzinom
Belzutifan darf während der Schwangerschaft nicht angewendet werden, es sei denn, dass eine Behandlung mit Belzutifan aufgrund des klinischen Zustandes der Frau erforderlich ist.
Von Hippel-Lindau-Syndrom(VHL)-assoziierte Tumoren
Belzutifan ist während der Schwangerschaft kontraindiziert (siehe Abschnitt 4.3). Tritt während der Behandlung mit Belzutifan eine Schwangerschaft ein, muss die Behandlung abgesetzt werden.
Stillzeit
Es liegen keine Daten von Belzutifan oder seinen Metaboliten zu einem Übergang in die Muttermilch, deren Auswirkungen auf das gestillte Kind oder auf die Milchproduktion vor. Aufgrund des Potenzials von schwerwiegenden Nebenwirkungen bei gestillten Kindern wird Frauen geraten, während der Behandlung mit Belzutifan und für mindestens 1 Woche nach der letzten Dosis nicht zu stillen.
Fertilität
Basierend auf tierexperimentellen Befunden kann Belzutifan die Fertilität bei zeugungsfähigen Männern und gebärfähigen Frauen beeinträchtigen (siehe Abschnitt 5.3). Patienten sollten auf dieses potenzielle Risiko hingewiesen werden. Die Reversibilität der Auswirkungen auf die Fertilität ist unbekannt.
Belzutifan hat einen geringen Einfluss auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen. Nach der Einnahme von Belzutifan können Schwindel und Ermüdung/Fatigue auftreten (siehe Abschnitt 4.8).
Den Patienten ist anzuraten, kein Auto zu fahren und keine Maschinen zu bedienen, bis sie sich gewiss sind, dass die Belzutifan-Therapie dies nicht negativ beeinflusst.
Zusammenfassung des Sicherheitsprofils
Die Sicherheit von Belzutifan wurde in klinischen Studien bei 576 Patienten mit fortgeschrittenen soliden Tumoren und VHL-Syndrom-assoziierten lokalisierten Tumoren untersucht, die einmal täglich mit 120 mg Belzutifan behandelt wurden. Die mediane Dauer der Exposition gegenüber Belzutifan betrug 9,2 Monate (Spanne: 0,1 bis 55,4 Monate).
Die häufigsten Nebenwirkungen unter der Behandlung mit Belzutifan waren Anämie (84,2 %), Ermüdung/Fatigue (42,7 %), Übelkeit (24,1 %), Dyspnoe (21,4 %), Schwindelgefühl (17,9 %) und Hypoxie (16,3 %).
Die häufigsten Nebenwirkungen des Grades 3 oder 4 waren Anämie (28,8 %) und Hypoxie (12,2 %).
Die häufigsten schwerwiegenden Nebenwirkungen waren Hypoxie (7,1 %), Anämie (4,7 %) und Dyspnoe (1,2 %).
Die häufigsten Nebenwirkungen, die zu einer Unterbrechung der Belzutifan-Behandlung führten, waren Anämie (7,1 %), Hypoxie (5,4 %), Ermüdung/Fatigue (2,6 %), Übelkeit (2,4 %), Dyspnoe (1,7 %) und Schwindelgefühl (1,6 %). Die häufigsten Nebenwirkungen, die zu einer Dosisreduktion von Belzutifan führten, waren Hypoxie (6,3 %), Anämie (3,8 %) und Ermüdung/Fatigue (1,7 %). Die häufigste Nebenwirkung, die zum Absetzen der Belzutifan-Behandlung führte, war Hypoxie (1,4 %).
Tabellarische Zusammenfassung der Nebenwirkungen
Nebenwirkungen, die im gepoolten Datensatz für mit Belzutifan behandelte Patienten (n = 576) oder durch Anwendung nach Markteinführung gemeldet wurden, sind in Tabelle 2 aufgeführt. Diese Nebenwirkungen sind nach Systemorganklasse und Häufigkeit aufgelistet. Häufigkeiten sind wie folgt definiert: sehr häufig (≥ 1/10); häufig (≥ 1/100 bis < 1/10); gelegentlich (≥ 1/1 000 bis < 1/100); selten (≥ 1/10 000 bis < 1/1 000); und sehr selten (< 1/10 000).
Tabelle 2: Nebenwirkungen bei Patienten unter der Behandlung mit Belzutifan*
Systemorganklasse |
Alle Grade |
Grad 3 bis 4 |
Erkrankungen des Blutes und des Lymphsystems |
||
Anämie† |
Sehr häufig |
Sehr häufig |
Erkrankungen des Nervensystems |
||
Schwindelgefühl |
Sehr häufig |
- |
Gefäßerkrankungen |
||
Blutung‡# |
Sehr häufig |
Häufig |
Erkrankungen der Atemwege, des Brustraums und Mediastinums |
||
Dyspnoe |
Sehr häufig |
Häufig |
Hypoxie |
Sehr häufig |
Sehr häufig |
Erkrankungen des Gastrointestinaltrakts |
||
Übelkeit |
Sehr häufig |
Gelegentlich |
Allgemeine Erkrankungen und Beschwerden am Verabreichungsort |
||
Ermüdung/Fatigue |
Sehr häufig |
Häufig |
Untersuchungen |
||
Gewicht erhöht |
Häufig |
Häufig |
* Die in Tabelle 2 aufgelisteten Nebenwirkungshäufigkeiten können anteilig durch die zugrunde liegende Erkrankung bedingt sein. | ||
Beschreibung ausgewählter Nebenwirkungen
Anämie (siehe Abschnitt 4.4)
Anämie trat bei 83 % der Patienten mit fortgeschrittenem RCC auf, die Belzutifan erhielten, wobei 32 % eine Anämie Grad 3 und 0,5 % eine Anämie Grad 4 hatten. Die mediane Zeit bis zum Auftreten einer Anämie betrug 29 Tage (Spanne: Tag 1 bis 27 Monate). Von den Patienten mit einer Anämie erhielten 22 % nur Transfusionen, 20 % der Patienten nur ESAs und 14 % sowohl Transfusionen als auch ESAs. Die mediane Anzahl der den Patienten verabreichten ESA-Dosen betrug 6,5 (Spanne: 1 bis 87). Die Patienten erhielten ein ESA basierend auf ihrem Hämoglobinspiegel und nach Ermessen des Arztes (siehe Abschnitt 5.1).
Anämie trat bei 90,2 % der Patienten mit VHL-assoziierten Tumoren auf, die Belzutifan erhielten; 11,5 % der Patienten hatten eine Anämie Grad 3. Die mediane Zeit bis zum Auftreten von Anämien jeglichen Grades betrug 30 Tage (Spanne: Tag 1 bis 8 Monate). Von den Patienten mit Anämie erhielten 1,8 % nur Transfusionen, 16,4 % nur ESAs und 9,1 % der Patienten sowohl Transfusionen als auch ESAs. Die mediane Anzahl der den Patienten verabreichten ESA-Dosen betrug 5 (Spanne: 1 bis 35). Die Patienten erhielten ein ESA basierend auf ihrem Hämoglobinspiegel und nach Ermessen des Arztes (siehe Abschnitt 5.1).
Die Inzidenz einer Anämie Grad 3 nahm mit höherer Belzutifan-Exposition bei Patienten mit Hämoglobin-Ausgangswerten < 12 g/dl zu (siehe Abschnitt 4.4).
Hypoxie (siehe Abschnitt 4.4)
Hypoxie trat bei 15 % der Patienten mit fortgeschrittenem RCC auf, die Belzutifan erhielten, wobei 10 % der Patienten eine Hypoxie Grad 3 und 0,3 % der Patienten eine Hypoxie Grad 4 hatten. Von den Patienten mit Hypoxie wurden 70 % mit einer Sauerstofftherapie behandelt. Die mediane Zeit bis zum Auftreten einer Hypoxie betrug 31 Tage (Spanne: Tag 1 bis 21 Monate).
Hypoxie (Grad 3) wurde bei 1,6 % der Patienten mit VHL-assoziierten Tumoren berichtet, die Belzutifan erhielten. Die Zeit bis zum Auftreten einer Hypoxie betrug 56 Tage.
Meldung des Verdachts auf Nebenwirkungen
Die Meldung des Verdachts auf Nebenwirkungen nach der Zulassung ist von großer Wichtigkeit. Sie ermöglicht eine kontinuierliche Überwachung des Nutzen-Risiko-Verhältnisses des Arzneimittels. Angehörige von Gesundheitsberufen sind aufgefordert, jeden Verdachtsfall einer Nebenwirkung dem Bundesinstitut für Arzneimittel und Medizinprodukte, Abt. Pharmakovigilanz, Kurt-Georg-Kiesinger-Allee 3, D-53175 Bonn, Website: www.bfarm.de, anzuzeigen.
Es gibt keine spezielle Behandlung bei einer Überdosierung mit Belzutifan. Bei Verdacht auf eine Überdosierung ist die Gabe von Belzutifan gegebenenfalls zu unterbrechen und unterstützende Maßnahmen einzuleiten. Die höchste klinisch untersuchte Belzutifan-Dosis betrug 240 mg Gesamttagesdosis (120 mg zweimal täglich oder 240 mg einmal täglich). Bei einer Dosis von 120 mg zweimal täglich trat eine Hypoxie Grad 3 auf und bei 240 mg einmal täglich trat eine Thrombozytopenie Grad 4 auf.
Pharmakotherapeutische Gruppe: Antineoplastische Mittel, Andere antineoplastische Mittel, ATC-Code: L01XX74
Wirkmechanismus
Belzutifan ist ein Inhibitor des Hypoxie-induzierbaren Transkriptionsfaktors 2 alpha (HIF-2α). Bei normaler Sauerstoffsättigung wird HIF-2α zielgerichtet vom VHL-Protein abgebaut.
Eine Beeinträchtigung der VHL-Proteinfunktion führt zu einer Akkumulation von HIF-2α. Folglich wandert HIF-2α in den Zellkern und reguliert die Expression von Genen, die mit zellulärer Proliferation, Angiogenese und Tumorwachstum in Zusammenhang stehen. Belzutifan bindet an HIF-2α und blockiert bei Hypoxie oder Beeinträchtigung der VHL-Proteinfunktion die HIF-2α-HIF-1β-Interaktion, was zu einer verringerten Transkription und Expression von HIF-2α-Zielgenen führt.
Pharmakodynamische Wirkungen
Die zirkulierenden Plasmaspiegel von Erythropoetin (EPO) wurden bei Patienten als pharmakodynamischer Marker der HIF-2α-Hemmung überwacht. Es wurde beobachtet, dass die EPO-Reduktionen dosis-/expositionsabhängig waren und bei Expositionen, die mit Dosen über 120 mg einmal täglich erreicht wurden, einen Plateaueffekt zeigten. Die maximale EPO-Suppression trat nach 2 Wochen aufeinanderfolgender Belzutifan-Dosierung auf (mittlerer prozentualer Rückgang vom Ausgangswert um etwa 60 %). Die mittleren EPO-Spiegel kehrten nach 12-wöchiger Behandlung allmählich auf die Ausgangswerte zurück.
Unter der empfohlenen Belzutifan-Dosis (120 mg einmal täglich) gab es keine klinisch relevanten Auswirkungen auf das QTc-Intervall.
Klinische Wirksamkeit
Klinische Studie bei erwachsenen Patienten mit fortgeschrittenem Nierenzellkarzinom (RCC)
Die Wirksamkeit von Belzutifan wurde in LITESPARK-005, einer offenen, randomisierten, aktiv kontrollierten klinischen Phase-3-Studie, untersucht, in der Belzutifan mit Everolimus bei 746 Patienten mit nicht resezierbarem, lokal fortgeschrittenem oder metastasiertem klarzelligen Nierenzellkarzinom verglichen wurde, das nach einer sequenziellen oder kombinierten Therapie mit einem PD-1/L1-Checkpoint-Inhibitor und einer zielgerichteten VEGF-Therapie fortgeschritten war. Die Patienten konnten bis zu 3 vorherige Behandlungsschemata erhalten haben und mussten eine messbare Erkrankung gemäß RECIST v1.1 aufweisen. Von der Studie ausgeschlossen waren Patienten mit Hypoxie, aktiven ZNS-Metastasen und klinisch signifikanten Herzerkrankungen. Die Patienten wurden im Verhältnis 1:1 randomisiert und erhielten einmal täglich 120 mg Belzutifan oder 10 mg Everolimus oral. Die Randomisierung wurde nach den Risikokategorien des International Metastatic RCC Database Consortium (IMDC) (gut vs. intermediär vs. schlecht) und der Anzahl vorheriger zielgerichteter VEGF-Therapien (1 vs. 2 bis 3) stratifiziert.
Die Patienten wurden in Woche 9 ab dem Datum der Randomisierung, dann alle 8 Wochen bis Woche 49 und danach alle 12 Wochen radiologisch untersucht.
Von den 746 Patienten in LITESPARK-005 erhielten 369 Patienten zwei oder mehr Therapielinien, darunter ein PD-(L)1-Inhibitor und mindestens zwei zielgerichtete VEGF-Therapien. Die Ausgangsmerkmale dieser Patienten waren: Durchschnittsalter 63 Jahre (Spanne: 33 bis 82 Jahre), 40 % 65 Jahre oder älter; 11 % 75 Jahre oder älter; 79 % männlich; 78 % kaukasischer Herkunft; 12 % asiatischer Herkunft; 1 % afrikanischer oder afroamerikanischer Herkunft; 42 % ECOG-Performance-Status 0 und 56 % ECOG-Performance-Status 1. Vorherige Therapielinien: 17 % der Patienten hatten 2, 81% hatten 3 und 2 % hatten 4 vorherige Therapielinien. Die Patientenverteilung nach IMDC-Risikokategorien war 22 % gut, 66 % intermediär und 12 % schlecht.
Die primären Wirksamkeitsendpunkte waren das Überleben ohne Fortschreiten der Krebserkrankung (Progression Free Survival, PFS), bewertet durch eine zentrale Beurteilung (Blinded Independent Central Review, BICR) unter Verwendung von RECIST v1.1, und das Gesamtüberleben (Overall Survival, OS). Sekundäre Wirksamkeitsparameter umfassten die objektive Ansprechrate (Objective Response Rate, ORR) und die Ansprechdauer (Duration of Response, DOR) durch BICR unter Verwendung von RECIST v1.1.
In der Gesamtpopulation zeigte die Studie im Vergleich zu Everolimus in einer präspezifizierten Interimsanalyse (mediane Nachbeobachtungszeit von 13,5 Monaten [Spanne: 0,2 bis 31,8 Monate]) eine statistisch signifikante Verbesserung hinsichtlich PFS (HR: 0,75 [95 % KI 0,63; 0,90]; p-Wert 0,00077) und ORR (21,9 % vs. 3,5 %; p-Wert < 0,00001) bei Patienten, die randomisiert Belzutifan erhielten.
Tabelle 3 fasst die wichtigsten Wirksamkeitsendpunkte in der Subgruppe der Patienten in LITESPARK-005 zusammen, die zwei oder mehr Therapielinien, darunter ein PD-(L)1-Inhibitor und mindestens zwei zielgerichtete VEGF-Therapien, erhielten. Die Kaplan-Meier(KM)-Kurven für PFS und OS sind in den Abbildungen 1 und 2 dargestellt.
Tabelle 3: Wirksamkeitsergebnisse in LITESPARK-005 bei Patienten, die zwei oder mehr Therapielinien, darunter ein PD-(L)1-Inhibitor und mindestens zwei zielgerichtete VEGF-Therapien, erhielten
Endpunkt |
Belzutifan |
Everolimus |
PFS* |
||
Anzahl Patienten mit Ereignis n (%) |
127 (67,9 %) |
130 (71,4 %) |
Medianes† PFS in Monaten (95 % KI) |
4,6 (3,5; 7,3) |
5,4 (3,8; 6,5) |
Hazard-Ratio‡ (95 % KI) |
0,73 (0,57; 0,94) |
|
OS¶ | ||
Anzahl Patienten mit Ereignis n (%) |
128 (68,1 %) |
125 (68,7 %) |
Medianes† OS in Monaten (95 % KI) |
21,8 (17,4; 25,8) |
18,1 (14,2; 23,9) |
Hazard-Ratio‡ (95 % KI) |
0,94 (0,74; 1,21) |
|
ORR* % (95 % KI) |
24,1 % (18,1; 30,8) |
3,3 % (1,2; 7,0) |
Vollständiges Ansprechen n (%) |
5 (2,7 %) |
0 (0 %) |
Partielles Ansprechen n (%) |
40 (21,4 %) |
6 (3,3 %) |
Ansprechdauer* |
||
Mediane DOR in Monaten (Spanne) |
N. e. (1,9+; 23,1+) |
17,2 (3,8; 17,2) |
* Basierend auf der ersten präspezifizierten Interimsanalyse (mediane Nachbeobachtungszeit 13,2 Monate), bewertet durch BICR. | ||
Die mediane Zeit bis zum Ansprechen (Time to Response, TTR) bei Patienten in der Subgruppe von LITESPARK-005, die zwei oder mehr Therapielinien erhielten, darunter ein PD-L(1)-Inhibitor und mindestens zwei zielgerichtete VEGF-Therapien, betrug 3,7 Monate (Spanne: 1,7 bis 16,6) im Belzutifan-Arm und 3,0 Monate (Spanne: 1,8 bis 5,4) im Everolimus-Arm (mediane Nachbeobachtungszeit 13,5 Monate).
Abbildung 1: Kaplan-Meier-Kurve des Überlebens ohne Fortschreiten der Krebserkrankung nach Behandlungsarm in LITESPARK-005 bei Patienten, die zwei oder mehr Therapielinien erhielten, darunter ein PD-(L)1-Inhibitor und mindestens zwei zielgerichtete VEGF-Therapien*
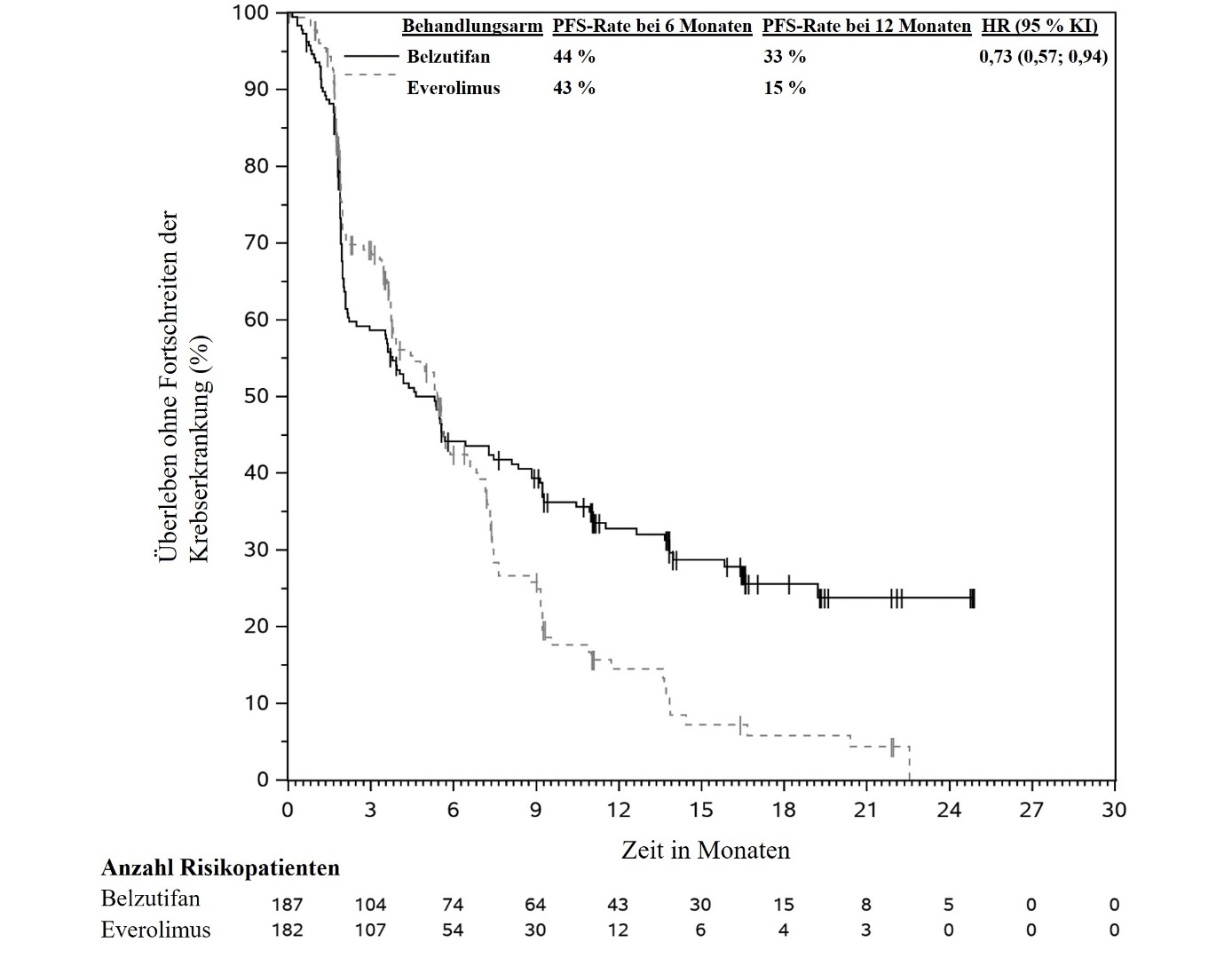
* Mediane Nachbeobachtungszeit 13,2 Monate
Abbildung 2: Kaplan-Meier-Kurve für das Gesamtüberleben nach Behandlungsarm in LITESPARK-005 bei Patienten, die zwei oder mehr Therapielinien erhielten, darunter ein PD-(L)1-Inhibitor und mindestens zwei zielgerichtete VEGF-Therapien*
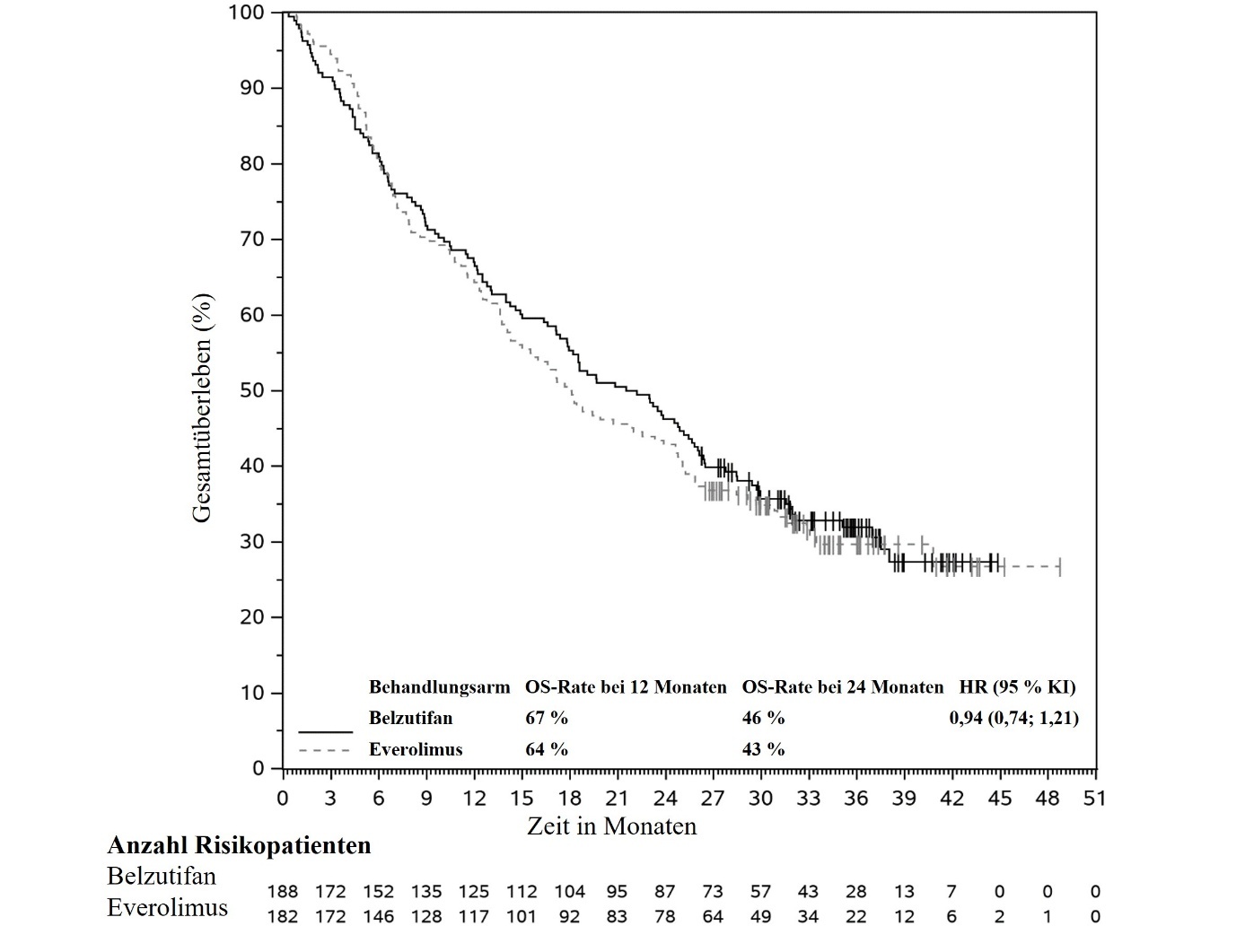
* Mediane Nachbeobachtungszeit 18,9 Monate
Klinische Studie bei erwachsenen Patienten mit von Hippel-Lindau-Syndrom(VHL)-assoziierten Tumoren
Die Wirksamkeit von Belzutifan wurde in LITESPARK-004, einer offenen klinischen Phase-2-Studie an 61 Patienten mit VHL-Syndrom untersucht, die mindestens einen messbaren soliden Tumor (gemäß RECIST v1.1 definiert) in der Niere hatten und die nicht sofort operiert werden mussten. Die Patienten konnten auch andere VHL-Syndrom-assoziierte Tumoren haben, wie Hämangioblastome des ZNS und pNET. Die Patienten erhielten einmal täglich Belzutifan in einer Dosis von 120 mg. Die Patienten wurden etwa 12 Wochen nach Beginn der Behandlung und danach alle 12 Wochen radiologisch untersucht. Die Behandlung wurde bis zum Fortschreiten der Erkrankung oder bis zu einer unzumutbaren Toxizität fortgesetzt. Die Patienten mussten einen ECOG-Performance-Status von 0 oder 1 aufweisen. Von der Studie ausgeschlossen waren Patienten, bei denen Anzeichen einer metastasierten Erkrankung (entweder RCC oder andere mit dem VHL-Syndrom-assoziierte Tumoren) vorlagen, bei denen ein sofortiger chirurgischer Eingriff zur Tumorbehandlung erforderlich war, bei denen innerhalb von 4 Wochen vor Studienbeginn ein größerer chirurgischer Eingriff durchgeführt wurde, bei denen innerhalb von 6 Monaten vor Gabe des Studienmedikaments ein größeres kardiovaskuläres Ereignis aufgetreten war oder bei denen eine vorherige systemische Behandlung von mit dem VHL-Syndrom-assoziierten RCC durchgeführt wurde.
Die 61 Patienten, die in LITESPARK-004 eingeschlossen wurden, hatten folgende Charakteristika: Durchschnittsalter 41 Jahre, 3,3 % 65 Jahre oder älter; 52,5 % männlich; 90,2 % kaukasischer Herkunft; 82,0 % hatten einen ECOG-Performance-Status von 0 und 16,4 % hatten einen ECOG-Performance-Status von 1. 77 % der Patienten hatten sich zuvor einer RCC-Operation unterzogen. Zu den weiteren mit dem VHL-Syndrom-assoziierten Tumoren bei Patienten zählten Pankreasläsionen (100,0 %), davon 36,1 % neuroendokrine Pankreastumoren, Hämangioblastome des ZNS (82,0 %) und Netzhauttumoren (19,7 %).
Der primäre Wirksamkeitsendpunkt für die Behandlung von VHL-Syndrom-assoziiertem RCC war die ORR, gemessen durch radiologische Bewertung gemäß RECIST v1.1, bewertet durch ein zentrales unabhängiges Prüfkomitee (Independent Review Committee, IRC). Weitere Wirksamkeitsendpunkte waren DOR und TTR. ORR und DOR wurden bei anderen VHL-Syndrom-assoziierten Tumoren als sekundäre Wirksamkeitsendpunkte bewertet.
Tabelle 4 fasst die Wirksamkeitsergebnisse für VHL-assoziierte RCC-Tumoren in LITESPARK-004 zusammen, basierend auf einer Interimsanalyse mit einer medianen Nachbeobachtungszeit von 49,7 Monaten.
Tabelle 4: Wirksamkeitsergebnisse für VHL-assoziierte RCC-Tumoren in LITESPARK-004
Endpunkt |
Belzutifan |
ORR* % (95 % KI) |
67,2 (54,0; 78,7) |
Vollständiges Ansprechen |
11,5 % |
Partielles Ansprechen |
55,7 % |
Dauer des Ansprechens† |
|
Median in Monaten (Spanne) |
N. e. (8,6+; 44,4+) |
% mit Dauer ≥ 12 Monaten |
100,0 % |
Zeit bis zum Ansprechen |
|
Median in Monaten (Spanne) |
11,1 (2,7; 41,2) |
Wirksamkeitsdaten zum Zeitpunkt einer medianen Nachbeobachtungszeit von 49,7 Monaten (Stichtag 3. April 2023). | |
Zu den Wirksamkeitsendpunkten für die Behandlung anderer mit dem VHL-Syndrom-assoziierten Tumoren gehörten ORR und DOR, bewertet vom IRC gemäß RECIST v1.1. Diese Ergebnisse sind in Tabelle 5 aufgeführt.
Tabelle 5: Wirksamkeitsergebnisse von Belzutifan bei anderen mit VHL-Syndrom-assoziierten Tumoren
Belzutifan |
||
Endpunkt |
Patienten mit auswertbaren Hämangioblastomen des ZNS |
Patienten mit auswertbaren neuroendokrinen Pankreastumoren |
ORR* % (95 % KI) |
48 % (33,7; 62,6) |
90,9 % (70,8; 98,9) |
Vollständiges Ansprechen |
8,0 % |
50,0 % |
Partielles Ansprechen |
40,0 % |
40,9 % |
Dauer des Ansprechens† |
||
Median in Monaten (Spanne) |
N. e. |
N. e. |
% mit Dauer ≥ 12 Monaten |
95,5 % |
100,0 % |
Wirksamkeitsdaten zum Zeitpunkt einer medianen Nachbeobachtungszeit von 49,7 Monaten (Stichtag 3. April 2023). | ||
Kinder und Jugendliche
Die Europäische Arzneimittel-Agentur hat für WELIREG eine Freistellung von der Verpflichtung zur Vorlage von Ergebnissen zu Studien in allen pädiatrischen Altersklassen bei Nierenneoplasmen und VHL-Syndrom gewährt (siehe Abschnitt 4.2 bzgl. Informationen zur Anwendung bei Kindern und Jugendlichen).
Zulassung unter „Besonderen Bedingungen“
Dieses Arzneimittel wurde unter „Besonderen Bedingungen“ zugelassen. Das bedeutet, dass weitere Nachweise für den Nutzen des Arzneimittels erwartet werden.
Die Europäische Arzneimittel-Agentur wird neue Informationen zu diesem Arzneimittel mindestens jährlich bewerten und, falls erforderlich, wird die Zusammenfassung der Merkmale des Arzneimittels aktualisiert werden.
Die Pharmakokinetik von Belzutifan ist bei gesunden Probanden und Patienten mit soliden Tumoren, einschließlich fortgeschrittenem RCC, ähnlich. Basierend auf einer populationsbezogenen pharmakokinetischen Analyse beträgt das simulierte geometrische Mittel im Steady State (CV %) Cmax bei Patienten, die mit 120 mg Belzutifan behandelt werden, 1,5 Mikrogramm/ml (46 %) und die AUC0 − 24 Std. 20,8 Mikrogramm•h/ml (64 %). Der Steady State wird nach etwa 3 Tagen erreicht.
Resorption
Nach einmaliger oraler Gabe von 120 mg Belzutifan traten maximale Plasmakonzentrationen (mediane Tmax) von Belzutifan 1 bis 2 Stunden nach der Gabe auf.
Einfluss von Nahrungsmitteln
Eine fett- und kalorienreiche Mahlzeit verzögerte die maximale Belzutifan-Konzentration um etwa 2 Stunden, hatte jedoch keinen Einfluss auf die Exposition (AUC). Nach dem Verzehr einer fett- und kalorienreichen Mahlzeit kam es zu einer leichten Abnahme von Cmax um 24 %, die jedoch klinisch nicht relevant war. Daher kann Belzutifan unabhängig von den Mahlzeiten eingenommen werden.
Verteilung
Basierend auf der populationsbezogenen pharmakokinetischen Analyse beträgt das mittlere Verteilungsvolumen (CV %) 120 l (28,2 %). Die Plasmaproteinbindung von Belzutifan beträgt 45 %. Das Blut-Plasma-Konzentrationsverhältnis von Belzutifan beträgt 0,88.
Biotransformation
Belzutifan wird primär durch UGT2B17 und CYP2C19 und in geringerem Maße durch CYP3A4 metabolisiert. Sowohl UGT2B17 als auch CYP2C19 weisen genetische Polymorphismen auf (siehe „Besondere Patientengruppen – Langsame duale UGT2B17- und CYP2C19-Metabolisierer“).
In-vitro-Bewertung von Arzneimittelwechselwirkungen
Belzutifan ist ein Substrat von UGT2B17, CYP2C19 und CYP3A4. Aktiver Transport ist kein wichtiger Faktor für die Disposition von Belzutifan. Belzutifan ist kein Inhibitor von CYP-Enzymen, UGT-Enzymen oder Transportern, mit Ausnahme von MATE2-K und möglicherweise MATE1. Belzutifan induziert nicht CYP1A2, jedoch induziert Belzutifan CYP2B6, CYP2C8 und CYP3A4 in einer konzentrationsabhängigen Weise (siehe Abschnitt 4.5).
Elimination
Basierend auf der populationsbezogenen pharmakokinetischen Analyse beträgt die mittlere (CV %) Clearance 5,89 l/h (60,6 %) und die mittlere Eliminationshalbwertszeit beträgt etwa 14 Stunden.
Nach oraler Verabreichung von radioaktiv markiertem Belzutifan an gesunde Probanden wurden etwa 49,6 % der Dosis im Urin und 51,7 % im Stuhl (hauptsächlich als inaktive Metaboliten) ausgeschieden. Etwa 6 % der Dosis wurden als Ausgangssubstanz im Urin wiedergefunden.
Linearität
Die Cmax- und AUC-Werte im Plasma stiegen in einem Dosisbereich von 40 mg bis 120 mg proportional an.
Besondere Patientengruppen
Nierenfunktionsstörung
Basierend auf einer populationsbezogenen pharmakokinetischen Analyse von Belzutifan bei gesunden Probanden und Krebspatienten wurden keine klinisch signifikanten Unterschiede in der mittleren Belzutifan-Exposition zwischen Probanden mit normaler Nierenfunktion und solchen mit leichter und moderater Nierenfunktionsstörung (untersucht durch die geschätzte glomeruläre Filtrationsrate [estimated Glomerular Filtration Rate, eGFR]) beobachtet. In einer speziellen pharmakokinetischen Studie erniedrigte sich die Belzutifan-Exposition (AUC0 − INF) bei Patienten mit terminalem Nierenversagen vor Hämodialyse um 6 % und erhöhte sich um 14 % nach Hämodialyse (siehe Abschnitt 4.2).
Leberfunktionsstörung
Basierend auf einer populationsbezogenen pharmakokinetischen Analyse von Belzutifan bei gesunden Probanden und Krebspatienten wurden keine klinisch signifikanten Unterschiede in der mittleren Belzutifan-Exposition zwischen Probanden mit normaler Leberfunktion (Gesamtbilirubin und AST ≤ ULN) und solchen mit leichter Leberfunktionsstörung (Gesamtbilirubin ≤ ULN und AST > ULN oder Gesamtbilirubin > 1 bis 1,5 x ULN und beliebiger AST) beobachtet. In einer speziellen pharmakokinetischen Studie erhöhte sich die Belzutifan-Exposition (AUC0 − INF) bei Patienten mit mittelschwerer Leberfunktionsstörung (Child-Pugh B) um 52 %. Patienten mit schwerer Leberfunktionsstörung wurden nicht untersucht (siehe Abschnitt 4.2).
Langsame duale UGT2B17- und CYP2C19-Metabolisierer
Patienten, die langsame duale UGT2B17- und CYP2C19-Metabolisierer sind, weisen eine höhere Belzutifan-Exposition auf, was die Häufigkeit und Schwere der Nebenwirkungen von Belzutifan erhöhen kann und engmaschig überwacht werden sollte (siehe Abschnitte 4.4 und 4.8).
Belzutifan wird hauptsächlich durch UGT2B17 und CYP2C19 metabolisiert. Die Aktivität dieser Enzyme variiert bei Personen mit verschiedenen genetischen Varianten, was sich auf die Belzutifan-Konzentrationen auswirken kann. Langsame Metabolisierer sind Personen, bei denen geringe bis keine Enzymaktivität angenommen wird. Bei Patienten, die langsame duale UGT2B17- und CYP2C19-Metabolisierer sind, kann CYP3A4 ein wichtiger Eliminationsweg sein.
Ungefähr 15 % der Kaukasier, 11 % der Lateinamerikaner, 6 % der Afroamerikaner, 38 % der Südasiaten und 69 % der Ostasiaten sind langsame UGT2B17-Metabolisierer. Etwa 2 % der Kaukasier, 1 % der Lateinamerikaner, 5 % der Afroamerikaner, 8 % der Südasiaten und 13 % der Ostasiaten sind langsame CYP2C19-Metabolisierer. Etwa 0,4 % der Kaukasier, 0,1 % der Lateinamerikaner, 0,3 % der Afroamerikaner, 3 % der Südasiaten und 9 % der Ostasiaten sind langsame duale UGT2B17- und CYP2C19-Metabolisierer. Die erwarteten Häufigkeiten in der japanischen Bevölkerung für langsame UGT2B17-, CYP2C19- und duale UGT2B17- und CYP2C19-Metabolisierer liegen bei etwa 77 %, 19 % bzw. 15 %. Die erwarteten Häufigkeiten in der US-Bevölkerung für die langsamen UGT2B17-, CYP2C19- und langsamen dualen UGT2B17- und CYP2C19-Metabolisierer liegen bei etwa 16 %, 3 % bzw. 0,5 %, basierend auf dem gemeldeten Anteil der US-Bevölkerung, der durch die wichtigsten Populationen/ethnischen Gruppen repräsentiert wird.
Die Auswirkungen von langsamen CYP2C19- und UGT2B17-Metabolisierern auf die Belzutifan-Exposition wurden in einer populationsbezogenen pharmakokinetischen Analyse untersucht. Basierend auf dem populationsbezogenen pharmakokinetischen Modell wird für Patienten, die langsame CYP2C19-, UGT2B17- oder langsame duale UGT2B17- und CYP2C19-Metabolisierer sind, eine 1,3-, 2,7- bzw. 3,3‑fache Exposition (Steady-State-AUC0 − 24 Std.) im Vergleich zu einem typischen Referenzpatienten (extensiver UGT2B17-Metabolisierer, extensiver/intermediärer CYP2C19-Metabolisierer) bei der empfohlenen Dosis prognostiziert. Basierend auf Expositions-Wirkungs-Analysen für Wirksamkeit und Sicherheit und dem Risiko-Nutzen-Profil wird keine Dosisanpassung empfohlen.
Auswirkungen von Alter, Geschlecht, ethnischer Zugehörigkeit, Population und Körpergewicht
Basierend auf einer populationsbezogenen pharmakokinetischen Analyse haben Alter (Spanne: 19 bis 90 Jahre), Geschlecht, ethnische Zugehörigkeit, Population und Körpergewicht (Spanne: 42,1 bis 166 kg) keinen klinisch bedeutsamen Einfluss auf die Pharmakokinetik von Belzutifan. Potenzielle Unterschiede in der Exposition zwischen den Populationen sind aufgrund unterschiedlicher Häufigkeiten metabolisierender Enzyme möglich (siehe „Besondere Patientengruppen – Langsame duale UGT2B17- und CYP2C19-Metabolisierer“).
Toxizität bei wiederholter Gabe
Studien zur oralen Toxizität bei wiederholter Gabe an Ratten und Hunden über einen Zeitraum von bis zu 3 Monaten zeigten bei allen Dosen eine Anämie, auch bei Expositionsspiegeln, die niedriger waren als die Expositionsniveaus beim Menschen. Obwohl die Anämie reversibel war, ist dies für Menschen relevant.
Karzinogenese
An transgenen rasH2-Mäusen wurde mit Belzutifan in Dosen von bis zu 600 mg/kg/Tag eine 26-wöchige Karzinogenitätsstudie durchgeführt, was einer Exposition von bis zum 28-Fachen der menschlichen Exposition bei der zugelassenen Dosis entspricht. Bei keiner Dosis wurden mit Belzutifan in Zusammenhang stehende neoplastische Befunde beobachtet und in der Studie wurde kein karzinogenes Risiko festgestellt.
Mutagenität
Belzutifan erwies sich in In-vitro-Tests zur bakteriellen Mutagenese und in Mikronukleus-Assays sowie bei einem In-vivo-Mikronukleus-Assay an Ratten bei 1,7‑facher menschlicher Exposition als nicht genotoxisch.
Reproduktionstoxizität
Es wurden keine Fertilitätsstudien mit Belzutifan durchgeführt. In der 3-monatigen Toxizitätsstudie mit wiederholter Gabe an Ratten wurden irreversible Hodenatrophie/-degeneration und Oligospermie bei Expositionen beobachtet, die niedriger waren als die menschliche Exposition bei der empfohlenen Dosis von 120 mg täglich. Bei Hunden wurde bis zu einer Exposition, die der menschlichen Exposition ähnlich war, keine Hodentoxizität beobachtet. Weder in den 3-monatigen Toxizitätsstudien an Ratten noch an Hunden gab es Befunde an weiblichen Fortpflanzungsorganen. HIF-2α spielt jedoch eine funktionelle Rolle im Uterus während der Embryoimplantation und der Entstehung einer Schwangerschaft bei Mäusen. Eine Hemmung von HIF-2α durch Belzutifan kann die Embryoimplantation beeinträchtigen und so die weibliche Fertilität beeinträchtigen.
In einer embryofetalen Entwicklungsstudie an Ratten verursachte die Gabe von Belzutifan während der Organogenese eine embryofetale Letalität von bis zu 100 %, ein reduziertes fetales Körpergewicht und fetale Skelettanomalien bei Expositionen, die ähnlich oder niedriger waren als die menschliche Exposition bei der empfohlenen Dosis von 120 mg täglich.
Tablettenkern
Hypromelloseacetatsuccinat
Mikrokristalline Cellulose (E 460)
Mannitol (E 421)
Croscarmellose-Natrium (E 468)
Hochdisperses Siliciumdioxid (E 551)
Magnesiumstearat (E 470b)
Filmüberzug
Poly(vinylalkohol) (E 1203)
Titandioxid (E 171)
Macrogol (E 1521)
Talk (E 553b)
Indigocarmin-Aluminiumlack (E 132)
Nicht zutreffend.
4 Jahre
Für dieses Arzneimittel sind keine besonderen Lagerungsbedingungen erforderlich.
Aluminium/Aluminium-Blisterpackungen
Packung mit 90 (3 Umkartons mit je 30) Filmtabletten
Nicht verwendetes Arzneimittel oder Abfallmaterial ist entsprechend den nationalen Anforderungen zu beseitigen.
Merck Sharp & Dohme B.V.
Waarderweg 39
2031 BN Haarlem
Niederlande
EU/1/24/1893/002
Datum der Erteilung der Zulassung: 12. Februar 2025
Januar 2026
Ausführliche Informationen zu diesem Arzneimittel sind auf den Internetseiten der Europäischen Arzneimittel-Agentur https://www.ema.europa.eu verfügbar.
Verschreibungspflichtig
Für weitere Informationen zu diesem Präparat wenden Sie sich bitte an die deutsche Vertretung des Zulassungsinhabers:
MSD Sharp & Dohme GmbH
Levelingstr. 4a
81673 München
Tel.: +49 (0) 89 20 300 4500
E-Mail: medinfo@msd.de
RCN: 000028241-DE
FACH-9000369-0001